◆連載◆薬物代謝に関わる腸内細菌~アレルギー疾患が急増した理由~ 第10回
1.ジゴキシンとエリスロマイシン、テトラサイクリンの相互作用のメカニズム
ジゴキシンの代謝には腸内細菌が関わっているのをご存じだろうか?ジゴキシンとエリスロマイシンの併用によってジゴキシンの血中濃度が上昇するといわれている。添付文書には「エリスロマイシン、クラリスロマイシン、テトラサイクリンとの併用によって腸内細菌叢*への影響による本剤の代謝の抑制、あるいは、P糖タンパク質を介した本剤の排泄の抑制により血中濃度が上昇するとの報告がある。」とされているが、クラリスロマイシンはCYP3A4阻害薬でありP糖タンパク質の阻害薬であることは今となっては誰でも知っているが、テトラサイクリンにはそのような阻害作用はないはずだ。ではエリスロマイシンはどうなんだろう、というのが今回のテーマだ。
エリスロマイシンとテトラサイクリンがジゴキシンの血中濃度を上げる報告はNew Engl J Medに掲載されたLindenbaumらの報告で抗生物質がジゴキシンを代謝する腸内細菌叢への影響を初めて明らかにした1)。内容はジゴキシン錠を投与し定常状態に達した10~17日目に、エリスロマイシンやテトラサイクリン系抗生物質を5日投与により、患者の10%で尿および糞便中のジゴキシン代謝物の排泄が阻害され、血清ジゴキシン濃度が2倍に上昇したという内容である。これは抗菌作用によって腸内細菌叢が変化し、嫌気性菌Eubacterium lentumによるジゴキシンの不活性物質への代謝(ジゴキシンのジヒドロジゴキシンへの代謝)が阻害されることによるという内容である(図1; 赤字および赤線部分に腸内細菌が関わっている)。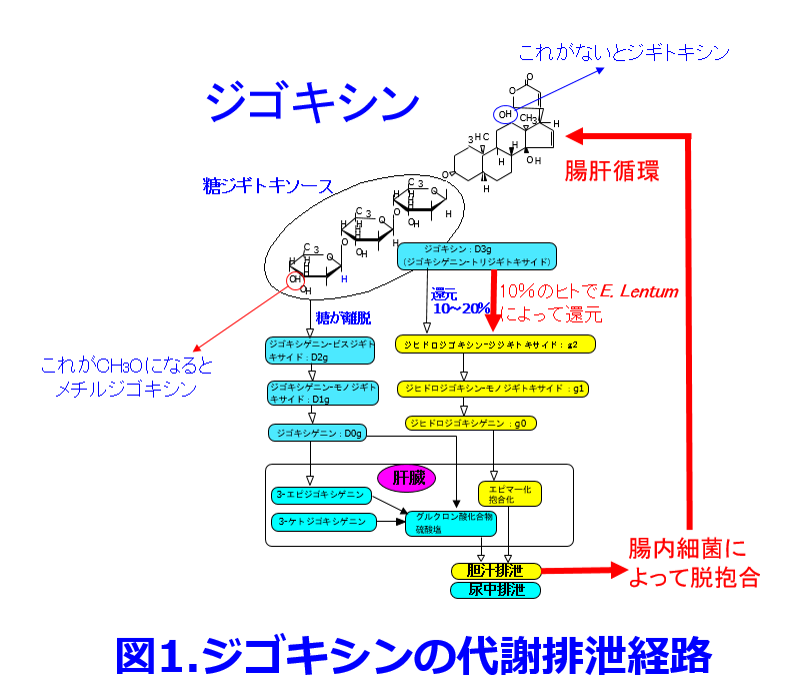 このためジゴキシン服用中の患者のうち腸内細菌としてE. lentumを持っている10%の人でジゴキシンの吸収が促進し、バイオアベイラビリティが上昇し、血中濃度が2倍になるというものである。
このためジゴキシン服用中の患者のうち腸内細菌としてE. lentumを持っている10%の人でジゴキシンの吸収が促進し、バイオアベイラビリティが上昇し、血中濃度が2倍になるというものである。
この論文のデータは非常にきれいであるが、ジゴキシンを代謝するE. lentumを常在菌として持っている人は10%にすぎず(報告によってはもっと高い報告もある)、腸内細菌叢の変化によって起こる血中濃度上昇は10人に1人しか起こりえないことになる。
クラリスロマイシンによる血中ジゴキシン濃度の上昇はジゴキシンが腎排泄性薬物であるため、近位尿細管のP糖タンパク質によるジゴキシンの排泄をクラリスロマイシンが阻害することによって起こると考えがちで、実際にそのような臨床報告もあった2)。筆者は白鷺病院時代に年間600件のジゴキシンのTDMをやっていた累積データから、クラリスロマイシンが併用された腎機能の廃絶した透析患者6名(うち4名は無尿)すべてで血中ジゴキシン濃度が平均3倍(1.8~4倍、非透析患者での相互作用も平均約3倍に上昇する(表))に上昇することを明らかにした(図2)3)。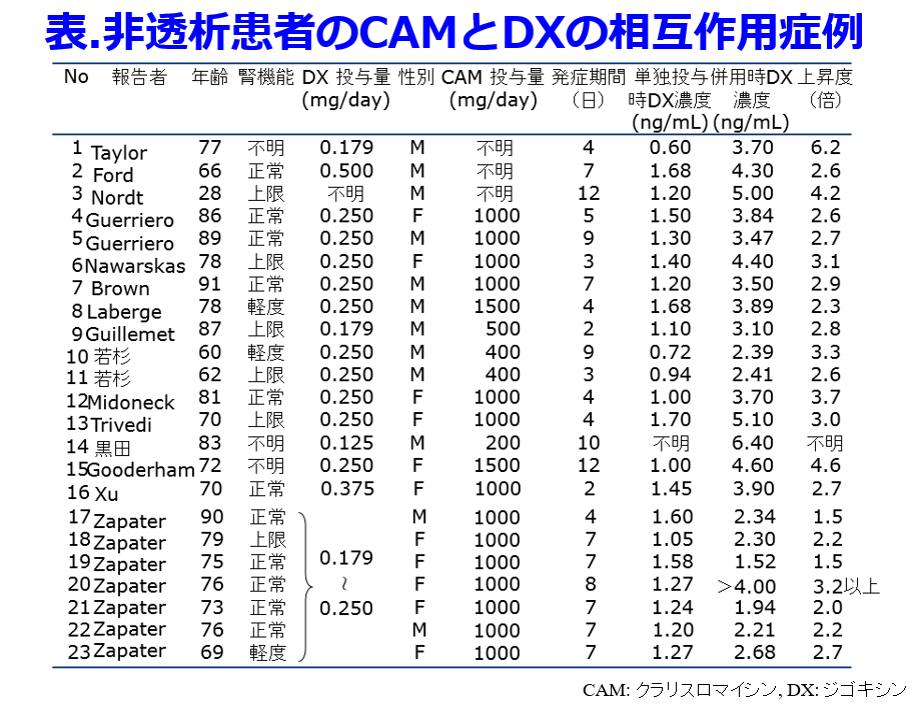
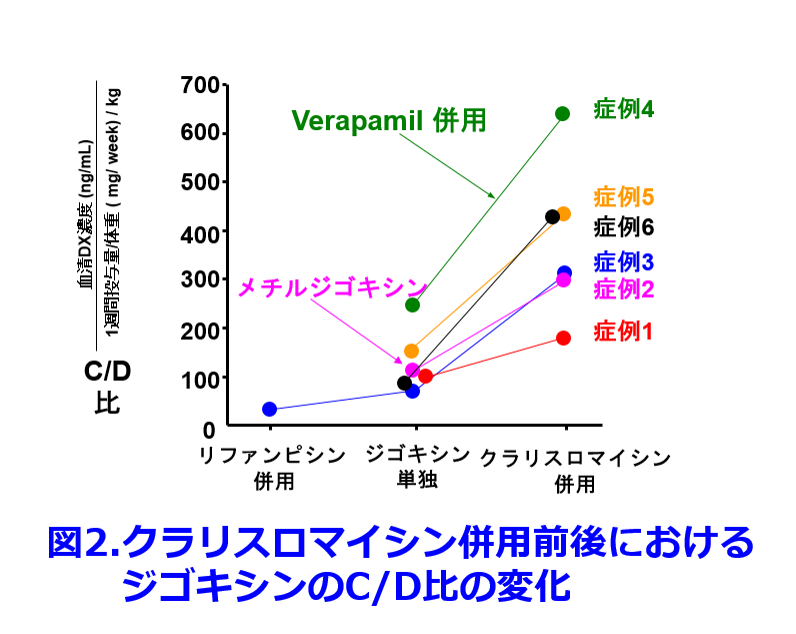 P糖タンパク質阻害薬のベラパミル(ワソラン?)が併用されていた症例4の血中濃度/用量比(C/D比)はもともと高く、症例3では結核によりP糖タンパク質を誘導するリファンピシンが投与されたときにはジゴキシン濃度は1/3に低下し、クラリスロマイシン併用によりリファンピシン中止時の3倍になるなど、クラリスロマイシンが併用された6名全員で明らかな血清ジゴキシン濃度の上昇が認められた。すなわちクラリスロマイシンとジゴキシンの相互作用はLindenbaumらの報告のように10%の確率で起こる相互作用ではなく、併用された6名全員に起こった相互作用であること、無尿の透析患者では尿細管機能も含め完全に腎機能が廃絶しているため、この相互作用はクラリスロマイシンが尿細管ではなく、胆管あるいは消化管のP糖タンパク質によるジゴキシンの排泄が阻害されているに違いないと考えている。
P糖タンパク質阻害薬のベラパミル(ワソラン?)が併用されていた症例4の血中濃度/用量比(C/D比)はもともと高く、症例3では結核によりP糖タンパク質を誘導するリファンピシンが投与されたときにはジゴキシン濃度は1/3に低下し、クラリスロマイシン併用によりリファンピシン中止時の3倍になるなど、クラリスロマイシンが併用された6名全員で明らかな血清ジゴキシン濃度の上昇が認められた。すなわちクラリスロマイシンとジゴキシンの相互作用はLindenbaumらの報告のように10%の確率で起こる相互作用ではなく、併用された6名全員に起こった相互作用であること、無尿の透析患者では尿細管機能も含め完全に腎機能が廃絶しているため、この相互作用はクラリスロマイシンが尿細管ではなく、胆管あるいは消化管のP糖タンパク質によるジゴキシンの排泄が阻害されているに違いないと考えている。
ジゴキシンとバラパミルは心房細動のレートコントロールによく併用されるため、非常に重要な相互作用であるが、ベラパミル錠240mg/日の併用によって透析患者のジゴキシン濃度は約2倍に上昇する。これに関してはジゴキシン服用者5名に経口ベラパミル最大用量の240mg/日を併用して腎クリアランスと胆汁クリアランス(胆汁を胆管からドレナージして採取する臨床試験は現在では倫理委員会を通らないのでは?)をクロスオーバー試験で示した報告で4)、腎クリアランスに変化はなかったものの胆汁クリアランスが有意に43%低下したことから、ジゴキシンの尿細管分泌よりも胆汁排泄、あるいは小腸での排泄が阻害されやすいのではないかということが推察できる(図3)。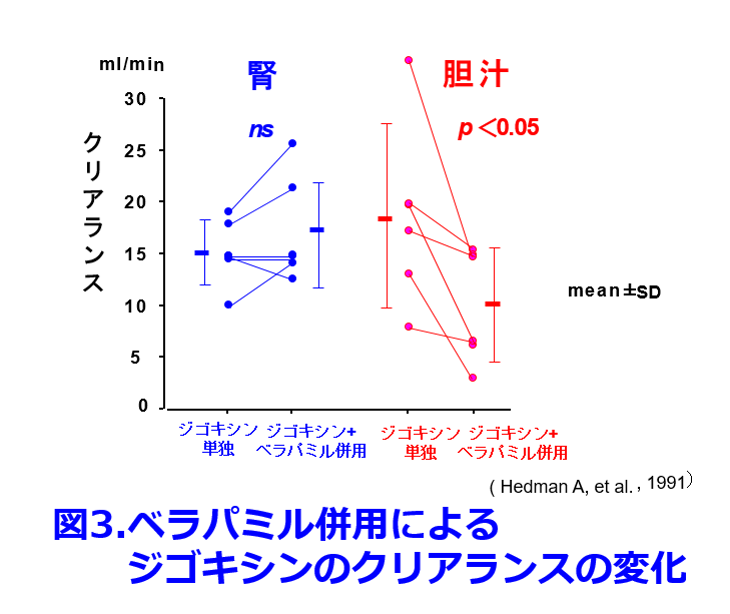 Lindenbaumらはこれ以降も権威の高い雑誌でこの現象について報告し続けたが、17年後にAm Fam Physician誌に「E. lentumを常在菌として持っていればジゴキシンの血中濃度が上がらないだろうが、1966年以来、私や私の仲間がこのような現象を見たことも聞いたこともない」というLetter to Editorが届いている5)。現在では同じマクロライド系のエリスロマイシンもクラリスロマイシンと同様、P糖タンパク質阻害のメカニズムと考えるのが妥当であろう。
Lindenbaumらはこれ以降も権威の高い雑誌でこの現象について報告し続けたが、17年後にAm Fam Physician誌に「E. lentumを常在菌として持っていればジゴキシンの血中濃度が上がらないだろうが、1966年以来、私や私の仲間がこのような現象を見たことも聞いたこともない」というLetter to Editorが届いている5)。現在では同じマクロライド系のエリスロマイシンもクラリスロマイシンと同様、P糖タンパク質阻害のメカニズムと考えるのが妥当であろう。
NOTE: 腸内細菌叢
抗菌薬シリーズ第6回でCD腸炎、偽膜性大腸炎の原因菌のクロストリジウム・ディフィシルが2016年以降、クロストリディオイディス・ディフィシルという名称に変わったと書いたが、腸内細菌叢の英名は以前はmicrofloraであったがこれでは植物を表すとして、新たにmicrobiota(遺伝情報まで含むとmicrobiome)に変わった。細菌は細胞核を持たない原核生物で、同じ微生物の中でも真核生物である真菌とは異なる分類になる。「細菌は細胞壁をもつので植物?」と思う方もいるかもしれないがこれらは全く別物で、生物は細菌を含む原核生物と真核生物に分かれ、学説によって異なるが真核生物はさらに動物界、植物界、原生生物界(真菌を含む菌界)などに分かれるという5界説で説明すると理解しやすいかもしれない。
2.腸肝循環する薬物代謝にも腸内細菌が関わっている
薬物代謝に関わる腸内細菌はジゴキシンに関しては疑わしい部分もあるが、腸内細菌が薬物代謝に関わっている例はこれだけではない。モルヒネが高齢者や腎機能低下患者で使いにくいのはM6G(モルヒネ-6-グルクロニド)というグルクロン酸抱合体が蓄積してせん妄をきたしやすいことによる。グルクロン酸抱合体は極性が高いため腎機能正常者であれば速やかに尿中に排泄されるが腎機能が低下すると蓄積しやすいためである。ただしそれだけではない。腎機能が低下して蓄積した抱合体は胆管のトランスポータによって胆汁排泄されやすいが、十二指腸に排泄された抱合体が回腸で腸内細菌の持つβグルクロニダーゼによって脱抱合され、再びモルヒネとして吸収されて肝臓で代謝されるという「腸肝循環」によって血中濃度が下がりにくくなることがある(図4)。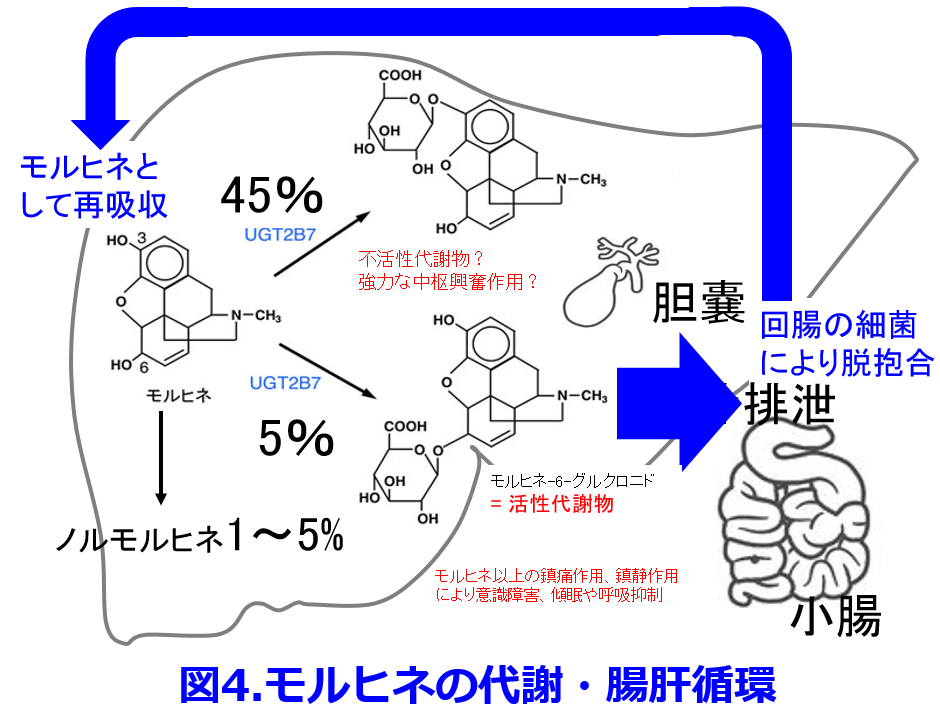 腸肝循環する薬物にはモルヒネのほかにも先述のジゴキシン(図1)、アセトアミノフェン、コルヒチン、エストロゲンなどの薬物のほかにもたくさんあるので本ホームページの「育薬に活用できるデータベースの 2.薬物動態の 4.腸肝循環する薬物」の一覧表およびその解説を見ていただきたい。さらに腎機能悪化の原因となるインドキシル硫酸、パラクレジル硫酸、トリメチルアミン-N-オキサイドなどのいずれの尿毒素uremic toxinも腸内細菌によって産生されているが、これについては次回、第11回で触れたいと思う。
腸肝循環する薬物にはモルヒネのほかにも先述のジゴキシン(図1)、アセトアミノフェン、コルヒチン、エストロゲンなどの薬物のほかにもたくさんあるので本ホームページの「育薬に活用できるデータベースの 2.薬物動態の 4.腸肝循環する薬物」の一覧表およびその解説を見ていただきたい。さらに腎機能悪化の原因となるインドキシル硫酸、パラクレジル硫酸、トリメチルアミン-N-オキサイドなどのいずれの尿毒素uremic toxinも腸内細菌によって産生されているが、これについては次回、第11回で触れたいと思う。
引用文献
1)Lindenbaum J, et al: N Engl J Med 305: 789-794, 1981
2)Wakasugi H, et al: Clin Pharmacol Ther 64: 123-128, 1998
3)Hirata S, et al: Int J Pharmacol Ther 43 (1): 30-36, 2005.
4) Hedman A, et al: Clin Pharamacol Ther 49: 256-262. 1991
5) Constantine PA: Am Fam Physician 57: 1239-1240, 1998

