2016年1月
TDMを始めてから薬剤師らしい仕事ができるようになった⑦
ダメ薬剤師が変われるきっかけ
AさんのTDMの成果は高く評価され、白鷺病院では他の抗不整脈薬、ジゴキシン、抗MRSA薬、抗てんかん剤など、TDMは幅広く実施されるようになった。TDMを実施することによって薬剤師に幅広い薬学的知識が身に付くと、TDM対象薬以外にもその知識は応用でき、より多くの薬物の有効かつ安全な投与が可能になった。そして「100床以下の小病院では学会発表なんて無理」なんて思っていた頃のことが嘘のように、薬剤科の学会発表数、文献執筆数は毎年、倍々ゲームのように増え続けた。93年ゼロだった文献数は94年1本、95年2本と増え続け、2003年には総説を加えると薬剤師5人で文献数は31本になった。学会発表や文献執筆は病院外へのアピールも大きいが、僕は病院内でのアピールが最も効果が高かったように思う。医師をはじめとした医療スタッフの信頼が得られ、その結果、薬剤師が薬剤師らしい仕事をできるように変われたことが一番のメリットだと考えている。
94年以前、僕たちは調剤しかできないダメ薬剤師だった。薬剤師が変わるきっかけはいろんなところにある。筆者にとってはAさんとの出会い、そして一生懸命、頑張ったTDMが成果を結んだことが変わるきっかけの1つと信じている。
(この原稿はファルマシア40(4): 304-306, 2004.に掲載されたものを改変しました)
TDMを始めてから薬剤師らしい仕事ができるようになった⑥
TDMとは?
AさんのTDMに際してはTDMの結果からさまざまな処方介入を行った。薬剤師が処方介入して、病状が悪化するとドクターの信頼を失い、TDMの依頼も来なくなる恐れがある。介入をした後は毎朝、毎夕、Aさんのベッドサイドに行った。そして処方変更後の効果の確認、副作用の観察を注意深く行った。結局、AさんのTDMを介して学んだことは「TDMは決して血中濃度を有効治療濃度域に直すためにやるのではなく、患者様を治すためにやっているのだということ。患者さんを見ないで血中濃度に対する薬学的コメントを書くべきではないこと」である。そしてそのポリシーは今も白鷺病院薬剤科で続いており、必ず服薬指導をしている薬剤師が血中濃度に対するコメントを書き、ドクターに報告している。試験室の薬剤師が血中薬物濃度を測定し、患者さんを見ないで薬学的コメントを書いている施設があるとすればそれはTDM(therapeutic drug monitoring)ではなくTDA(therapeutic drug assay/analysis)であると思う。これは筆者の勝手な解釈かもしれないが、AさんのTDMから学んだこと、「Monitoringにはその薬がちゃんと効いているかどうか、副作用は現れていないかどうかをmonitorするという意味もTDMには含んでいる」ということを信じている。
TDMを始めてから薬剤師らしい仕事ができるようになった⑤
Aさんのその後
Aさんの病状は改善し、疑問も解決した。しかし投与方法を変更しただけで副作用も不整脈も起こらなかったのは、奇跡としか言いようがない。危惧していた通り、約半年後にAさんは再び調子が悪くなり、50mgを1日2回投与ではコントロールできなくなって徐脈・頻脈が再発した。主治医は仕方なく50mgを1日3回投与に増量した。徐脈・頻脈は完全に消失したが、やはり視覚異常・食欲不振が再発した。再び文献検索した。何とか抗コリン作用を抑えられないものか?動物実験ではあったがジソピラミドの抗コリン作用はコリン剤で相殺できると書いてある文献を見つけた。しかしナパジシル酸アクラトニウムというマイルドな抗コリン剤を医師に勧めたが、ほとんど効果がなかった。結局、劇薬指定の強力なコリン剤である塩酸ベタネコールを1回15mg、1日3回ジソピラミドと一緒に投与するよう医師に勧めた。これは効きすぎた。下痢、腹痛、寝汗という強力な抗コリン作用が現れた。塩酸ベタネコールの最大作用発現時間は服用後1時間で作用持続時間は2時間と短い。これに対しジソピラミドはtmaxも遅く、透析患者では半減期が延長しているため、僕の投与設計ミスであった。結局1回7.5mgを1日6回という頻回投与することによってAさんの不整脈は副作用を全く起こすことなくコントロールできた。そのうちAさんは少量のベタネコールをジソピラミドのピーク濃度の直前に頓用すると副作用を防げるということを学んだ。
TDMを始めてから薬剤師らしい仕事ができるようになった④
薬剤師としての疑問解決
6月の終わりにAさんの症状は改善し退院した。しかし薬剤師としての疑問は残ったままである。
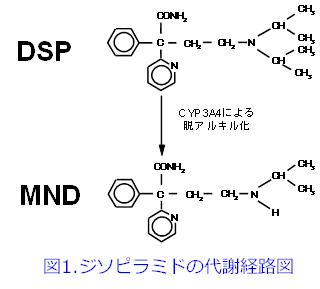
①非常に低い遊離型濃度なのにピーク値付近では不整脈を抑えられたこと。②総濃度は有効治療域内にあるのに強力な抗コリン作用が発現したこと。この2点の疑問を解く鍵はクロマトグラムにあった。腎機能正常者のクロマトグラムには小さなピークとしてしか現れないジソピラミドの前のピークが必ず、Aさんのクロマトグラムでは振り切れるくらいの巨大ピークとして現れるのだ。使用しているカラムはODSカラム、つまり逆相分配クロマトであるため、水溶性のものほどretention timeが早い。「腎臓は水溶性薬物を排泄する。肝臓は腎臓で排泄されやすいように薬物を極性の高い代謝物に変換する。そのため代謝物は親化合物よりも極性が高い。」と、ある薬物動態の教科書に書いてあったことを思い出した。ジソピラミドの代謝経路を調べた。ラッキーなことに1つの経路しかない。脱アルキル化されてmono-N-dealkyldisopyramide(MND)になる。インタビューフォームによるとMNDには活性があるらしい(図1)。
早速、2つの原著論文を取り寄せると同時にジソピラミドを製造しているフランスのルセルに英文でMNDの原末を取り寄せるべく手紙を書いた。取り寄せた文献によると動物の様々な不整脈モデルでジソピラミドの1/4から同等の抗不整脈作用を持つことが明らかになった。これで①の疑問は解決するかもしれない。そしてさらにMNDの抗コリン作用についてPubMedを使って文献検索した。ある文献のAbstractを見て思わず鳥肌が立った。「MNDは親化合物の24倍の抗コリン作用を有する」と書いてあった。これで②の疑問も解決するかもしれない。9月のはじめになってようやくMNDの原末がフランスから届いた。早速、HPLCに注入した。そして見事、Aさんのクラマトグラムで必ずジソピラミドの前に現れた巨大ピークと一致した(図2)。

これで薬剤師としての疑問は何とか解決できた。つまり①非常に低い遊離型濃度なのにピーク値付近では不整脈を抑えられたのはMNDに抗不整脈作用があったため、②総濃度は有効治療域内にあるのに強力な抗コリン作用が発現したのはMNDの抗コリン作用が強力であったためと考えた。
TDMを始めてから薬剤師らしい仕事ができるようになった③
TDMの結果から投与設計
総濃度でのトラフ値は0.75、ピーク値は2.87µg/mL、AAG濃度は103〜127mg/dLと健常者の約2倍あったため、蛋白結合率は約85%と高く、遊離型濃度はトラフ値が0.09、ピーク値は0.40µg/mLと低かった。この結果には薬剤師として大きな疑問が2つ生じた。①このような低い遊離型ピーク濃度では不整脈を抑えられないはずなのにピーク値付近では不整脈が完全に抑えられていたこと。②総濃度は有効治療域(2〜5µg/mL)内にあるのにピーク値付近では通常では起こりえない強力な抗コリン作用が発現していたことである。
トラフ値が低すぎたために徐脈・頻脈が現れ、ピーク値が高すぎたために視覚異常・食欲不振が発現するというAさんの病態から、投与方針は容易に決まった。ピーク値/トラフ値比をできるだけ大きくするためには少量頻回投与するべきである。至急50mgのカプセルを購入し、1日2回投与してもらうよう医師に勧めた。思った通り、ピーク値は下がり、トラフ値は上がった。そして奇跡的にAさんの徐脈・頻脈は1日中治まり、視覚異常・食欲不振も全く消失した。まさに奇跡であった。いくら内科医がAさんの投与方法を変更してもコントロールできなかった不整脈と副作用を薬剤師がTDMを実施することで完全にコントロールでき、退院できたのである。しかし薬剤師としての2つの疑問は残ったままだった。
TDMを始めてから薬剤師らしい仕事ができるようになった②
臨床経過を追う
入院当初、Aさんはジソピラミドカプセル100mgを1日1回投与されていた。そのうち不整脈が起こったため、主治医は100mgを1日2回投与に変更すると、徐脈・頻脈は完全に抑えられたが、案の定、視覚異常・食欲不振が現れた。100mg/日と200mg/日の1日おき投与を行ったが、視覚異常・食欲不振は持続し、100mgを1日1回投与に戻しても視覚異常・食欲不振は持続したため、主治医は100mgを28時間おきに投与するという変則処方を行った。今度は恐れていた徐脈・頻脈が現れた。結局、処方は入院当初の100mgを1日1回投与に戻ったが、Aさんの症状を観察していると視覚異常・食欲不振と徐脈・頻脈は決して同時には起こっていないことがわかった。ジソピラミドのtmaxは約3時間。ヒステリシスがあったとしても服用して3〜4時間が最大効果を示すと予測されるが、その時間帯では必ず視覚異常・食欲不振が起こっていた。そして次回服用前あたり、つまり血中濃度が最低になるトラフ値付近では必ず徐脈・頻脈が現れるのである。ここで初めてTDMの実施を決意した。その前にジソピラミドの薬物動態について調べた(表)。腎排泄型であるため半減期は延長しているはず。ジソピラミドは塩基性薬物であるため、アルブミンではなくα1-酸性糖タンパク質(AAG)と結合する。AAGの絶対量はアルブミンの1/40しかないため、ジソピラミドとの結合は容易に飽和する。そのため、蛋白結合率は5〜65%と幅広い。となると総濃度のトラフ値とピーク値だけでは効果の指標にならない。遊離型ジソピラミド濃度を測定するため限外濾過膜を購入し血清AAG濃度も測定した。遊離型濃度は低濃度であるため、師と仰ぐ上野和行先生(現新潟薬科大学教授)に教えを請い、HPLC法によって血清ジソピラミド濃度を測定した。

TDMを始めてから薬剤師らしい仕事ができるようになった①
服薬指導をはじめたきっかけ
1994年の4月になり100床以下の病院でもやっと薬剤管理指導業務の算定ができるようになった。病院の大小によって薬剤師の質が決まるものではない。小さな病院という理由だけで「病棟における服薬指導業務」ができないというのは理不尽な決まりであったが、そんなことを恨んでいても何も始まらない。僕たちは「100床以下」という枠が取り去られてから、すぐさま「病棟服薬指導業務」を開始した。そんな時に出会ったのが透析歴20年以上で腹膜透析施行中の40歳台の主婦Aさん。洞不全症候群といって、洞結節やその周辺の障害が元で、心拍数が40に落ちたり180まであがったりを繰り返す、いわゆる徐脈・頻脈症候群を呈していた。主治医はペースメーカーの植え込みを勧めたが、ある宗教上の理由から手術をかたくなに拒むため、内科療法として抗不整脈薬を投与せざるを得なかった。循環器内科医の診断によりVaughan Williams分類Ⅰa族のジソピラミド(リスモダン®)が有効であろうということで投与された。ジソピラミドはAさんに実によく効いたが、同時に副作用も強力に現れた。ジソピラミドの主な副作用は抗コリン作用に基づくもの。口渇や、便秘などは耐えられる副作用であるが、Aさんに発現する抗コリン作用は強力で、ジソピラミドの投与量を増やすと視調節障害が現れ、目を開けているとピントが合わないため、食欲不振になり、やがてほとんど食事が摂れなくなった。副作用がきついので、他剤に変更すると効果がない。仕方なく減量してジソピラミドを投与すると徐脈・頻脈が現れる。そして増量すると視覚異常・食欲不振が現れる。こんなことの繰り返しで抗不整脈薬療法がうまくいかないため、この1年間Aさんは入退院を繰り返してきた。筆者が服薬指導をはじめたのはAさんが再入院した94年の5月のことである。
新年のご挨拶
あけましておめでとうございます。
旧年中はひとかたならぬご厚誼を賜りまして、大変ありがとうございました。
今年から臨床薬理学分野は大学院生が2名になり、大所帯になります。1月~5月の育薬フロンティアセミナーは1月12日のバイタルサインの測定から始まります。特に保険薬局の先生方には薬を理解するためにも参加していただければ幸いです。
昨年、日本腎臓病薬物療法学会の会員数は1450名を超え、法人化も達成しました。これからは学会を上げての調査・研究活動、国際交流による意見交換も進めていきたいと思います。
2015年に作成された日本腎臓学会の薬剤性腎障害ガイドライン、日本化学療法学会の抗菌薬TDMガイドライン、日本TDM学会・日本循環器病学会の循環器TDMガイドラインの作成に関わりましたが2016年にはそれらが公開されます。
そして平田も今年で62歳。もう熊本大学に在籍できる時間もわずかになりました。今年は老体に鞭打って2月には熊本マラソンに挑みます。2017年には熊本市民会館崇城大学ホール・国際交流会館で第3回日本医薬品安全性学会、2019年には新設された熊本城ホールを中心に第13回日本腎臓病薬物療法学会を開催します。まだまだ老けてはいられません。この年になってこれだけのやりがいのある仕事に巡り合えるのは本当に幸せだと思います。そしてここまでやって来られたのも多くの人に支えられて来たからに違いありません。
今年も平田は精いっぱい頑張りますので、本年もなにとぞよろしくお願いいたします。
皆様に幸多き年となりますように。
あぁ、呆けるまでにもう一度カープの日本一を見てみたい・・・・・。
 平成28年元旦
平成28年元旦

