薬剤師塾Q&A
第22回 基礎から学ぶ薬剤師塾 Q&A
第 22回 基礎から学ぶ薬剤師塾 Q&A
慢性心不全とその治療薬
~これからはFantastic Fourの時代~
チャットでの質問
荒木脳神経外科病院薬剤部 戸田智美先生
Q.脳梗塞患者への持参薬継続としてSGLT2阻害薬の継続は可能でしょうか。
A.「脳梗塞を起こした患者さんの持参薬の中にSGLT2阻害薬が入っていたが、継続しても大丈夫か?」という質問と理解しました。SGLT2阻害薬の重要な副作用として脱水があり、それによって脳梗塞が起こることを懸念されているのかもしれませんが、SGLT2阻害薬による脱水は投与初期の利尿作用による血液濃縮によって脳梗塞を起こすことがあり得ます。ただしSGLT2阻害薬による利尿作用はNa利尿と糖利尿による尿量増加によりますが、この尿量増加はカナグリフロジンでは1日のみで、2日目以降は利尿作用が消失します(Tanaka H, et al,: Adv Ther 2017; 34: 436-51)。エンパグリフロジンの利尿作用は4日後も減少しませんが、この報告では全員ループ利尿薬が投与されており(Damman K, et al: Eur J Heart Fail. 2020 Apr;22(4):713-722. doi: 10.1002/ejhf.1713.)、エンパグリフロジンはフロセミドと相乗作用を示します。フロセミドとの併用で6週間以降も利尿作用は持続するするが、Na排泄は変化がなかったと報告されています(Mordi M, et al: Circulation 2020 Nov 3;142(18):1713-1724.)。
まとめますと、SGLT2阻害薬によるブドウ糖排泄作用は持続しますが、Na排泄量は10日程度持続するものの、それ以降は低下し1か月後にはプラセボ群と差がなくなります。ということで本題に戻りますが、SGLT2阻害薬は利尿作用がありますが、本症例が1か月以上投与されていれば、利尿作用は消失し、SGLT2阻害薬は心血管病変の発症を低下させますので、継続投与は問題ないというか、推奨されるかもしれません。ただし、この症例にループ利尿薬が併用されていれば(脳梗塞を発症した症例には通常、入院していない限りループ利尿薬を投与はしないと思いますが)脱水による脳梗塞を起こさないよう循環器医と相談のうえ、こまめな飲水指導をして投与を継続する必要があると思います。
アンケートでの質問
北九州宗像中央病院 高田由美子先生
Q.66歳男性、糖尿病性腎臓病で糖尿病外来に通院して3年になります。eGFRは29と30を切ってしまいました。今はグラクティブ(シタグリプチン)を50mg服用中ですが、この先、このままでいいのか、SGLT2阻害薬に変えなくていいのか心配です。どのようにお考えになりますか。
A.僕自身はDPP-4阻害薬をあまり評価していません。血糖は下げますが糖尿病性腎臓病の腎予後や先生予後を改善するという効果は証明されていないからです。でもSGLT2阻害薬を投与するには腎機能が高度腎障害のステージ4では、腎に作用するこの薬の効果が100%発揮できないと思いますが、効果が期待できないわけでもありません。平田は個人的には末期腎不全(eGFR<15mL/min/1.73m2)になっても、透析導入までは継続していいのではないかと思っています。 RAS阻害薬が併用されていれば血圧の下がりすぎに配慮してARNIに変更する(ただし腎保護の適応はありません)、腎機能がこのレベルになると高カリウム血症が怖いので場合によってはケイキサレートやロケルマを併用しつつMRAを併用するなど、腎臓内科医と相談してベストな薬物療法を考えるとよいと思います。
東京歯科大学市川総合病院 薬剤部の平井さやか先生
Q.最近ではダパグリフロジンでフレイル患者に使用した場合の論文がでており、フレイル患者でも比較的安全に使用できるのではないかという話も耳にします。フレイル患者には慎重に使用すべきであると考えますが、平田先生は避けたほうがよいというお考えでしょうか。
A.海外の論文で確かにフレイルの心不全患者でSGLT2阻害薬の有効性が示されたという報告があります。DAPA-HF試験のサブ解析で、ダパグリフロジンは、フレイル指数(0から1)にかかわらず、心不全の悪化や心血管死のリスクを減少させたことが報告されています(Butt JH, et al: Ann Intern Med. 2022 Jun;175(6):820-830. doi: 10.7326/M21-4776.)。ただしこの論文の内容をよ~く精査するとClass1(フレイルのない患者)のBMIは平均26.9、Class2のフレイル患者で平均28.9、Class3の強度フレイル患者の平均BMIはなんと30.6なのです(175cmで体重93~4kgに相当します)。白人・黒人ともにインスリン分泌能が高いため、これだけ太ったフレイル患者が多数を占めているのです。そりゃBMI30の患者にSGLT2阻害薬を投与すれば、グルカゴン/インスリン比が上がって体脂肪をケトン体に変換してエネルギーにしますので、体脂肪率がみるみる減って、動くのが楽になり、心不全も軽快するよねと思ってしまいました。
ただし欧米人とアジア人は異なります。痩せ気味の日本人のフレイル高齢者ではSGLT2阻害薬は尿糖を排泄することによって、体脂肪だけでなく、さらに筋肉量が減少してサルコペニアになってしまう危険性があります。しかもフレイルの高齢女性だと性器感染症も懸念されますので、平田は痩せが特徴的な日本人の高齢フレイル患者にはSGLT2阻害薬は投与を避けた方が無難だと考えています。
金沢医科大学病院薬剤部 高多瞭治先生
Q.大変勉強になりました。ありがとうございます。心不全(HFrEF)の透析患者さんに対して、ARNIやβブロッカーは積極的に使用していただくように医師とディスカッションを行っております。SGLT2阻害薬に関しては、透析患者さんでは効果が期待できないため投与は検討されませんが、MRAに関しては少し迷うところがあります。心臓のアルドステロン受容体遮断による心臓の線維化や心肥大の抑制は期待できますでしょうか?添付文書上はスピロノラクトンなどは禁忌であり、適応としても薬剤選択に苦慮します。何かご存知のエビデンスがありましたらご教授ください。
A.MRAは利尿作用、Na排泄促進作用などの腎臓への作用を介した効果が透析患者の心不全ではあまり期待できない可能性があります
スピロノラクトンに関してはPubMed検索では透析患者に投与した大規模研究はなく、少人数であまりレベルの高くない医学雑誌のものが多いのですが、左室肥大の改善、左室駆出率の上昇、心血管機能が改善したという報告が散見されます。それらのうちRCT>のメタ解析では全死亡や左室肥大やEFの改善が認められましたが、アジア人では25mgの低用量で有効性が高かったものの副作用も多かったことが記載されていました(Liu J, et al: Front Med (Lausanne). 2022 Mar 17;9:828189. doi: 10.3389/fmed.2022.828189. eCollection 2022.)。
医中誌検索では大学の腎臓内科医の先生が臨床透析誌38: 29-34, 2022に「ミネラルコルチコイド受容体拮抗薬では,抄録に透析患者においても有用である可能性が示されている」と書かれていました。
佐賀大学医学部附属病院 橘川奈生先生
Q.エンレストには蛋白尿減少効果はございますでしょうか。もともとタンパク尿がありARBを内服していた患者がが、ARBからエンレストに切り替えた場合、タンパク尿が増えますでしょうか。ご教示いただけますと幸いです。よろしくお願いいたします。
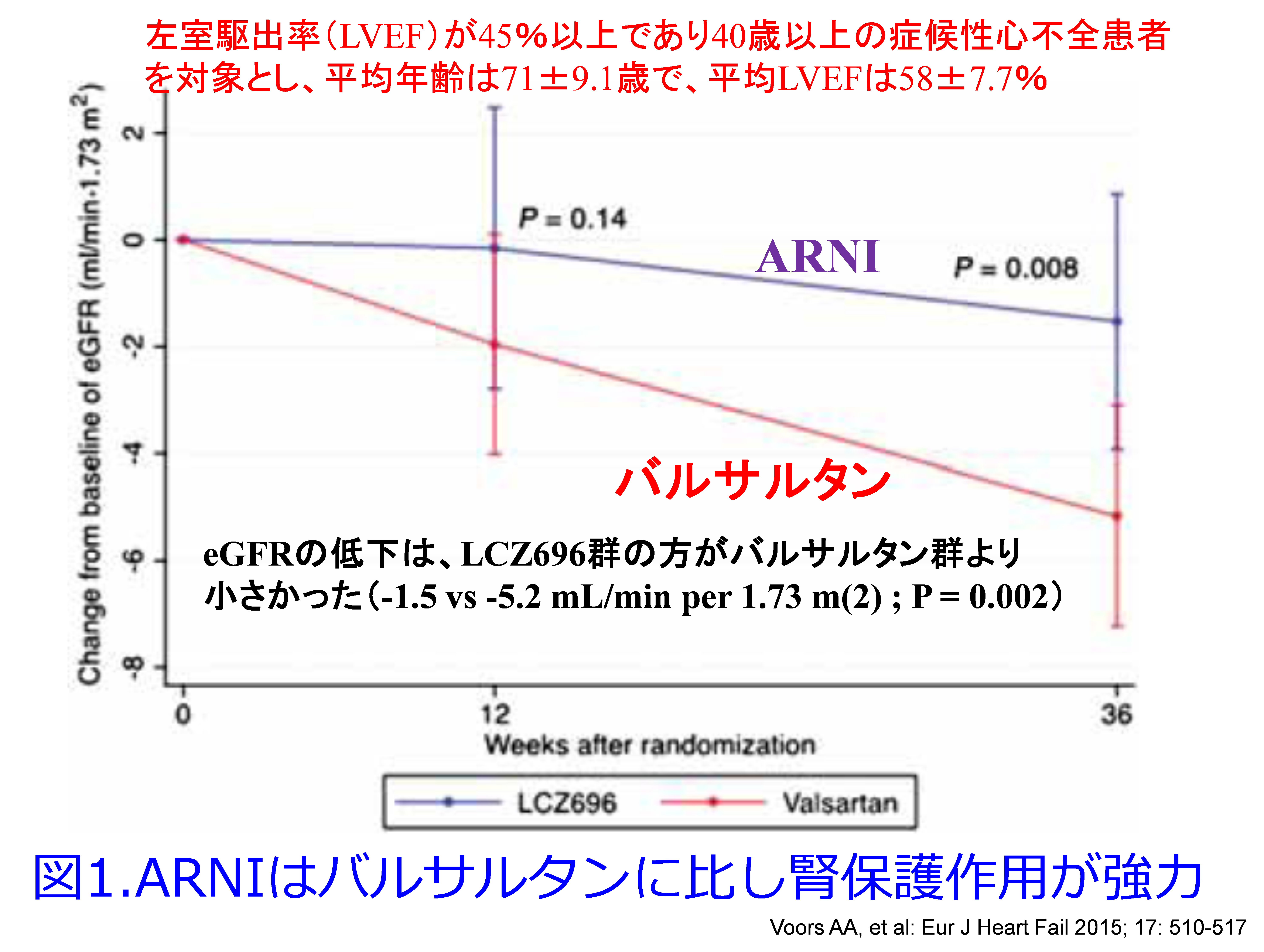
A.エンレストはバルサルタン群に比し、有意にアルブミン尿を増加させるという報告が確かにあります(Voors AA, et al: Eur J Heart Fail 2015; 17: 510-517)。それによると36週間後のARNI群の腎機能悪化は-1.5mL/min/1.73m2、バルサルタン群は-5.2mL/min/1.73m2でARNIの方が有意に腎機能悪化速度が緩やかでした(調整後のP = 0.002)。ARNIの尿中アルブミン/Cr比の幾何平均値はARNI群で増加した(2.1-4.0mg/mmol)のに対し、バルサルタン群では横ばいに推移し(1.5-2.6mg/mmol、36週間の差に関するP=0.016)、2群間で尿中アルブミン/クレアチニン比に有意差が生じました。これって2.1-4.0mg/mmolは18.6-35.4mg/gCrにあたり、1.5-2.6mg/mmol は13.3-23mg/gCrにあたります。尿中アルブミンは30mg/gCr未満が正常ですので、ARNI群はバルサルタン群に比し有意にアルブミン尿を増やしたのは確かですが、単位に騙されました。アルブミン尿はARNIを投与しても、ほぼほぼ正常域内です。だから正解はわずかにアルブミン尿は増えますが、増えたところでほぼ正常域内ですから、あまり心配ないように思っています。
第21回 基礎から学ぶ薬剤師塾 Q&A
第 21回 基礎から学ぶ薬剤師塾 Q&A
薬剤性腎障害を防ぐ
~Quadruple whammyを防げ!~
薬剤師塾は、もともと芦屋のI&H本社の大会議室で対面でのライブ形式で行おうと思っていましたが、コロナ対策のためオンラインで行っています。薬剤師塾にライブで参加している皆さんには、できるだけ熱いディスカッションをしていただき、薬剤師塾を盛り上げていただきたいと思います。どうしても自信のない方は所属・氏名、質問内容をチャットに記載してください。何も質問が出なければ、一方向の講演になってしまい、再放送を聞いている方は全く面白くありませんし、私もやりがいがありません。ですから、私の講演を聞いている間に不明な点やご意見などがあれば、積極的に質問して、どうか薬剤師塾を盛り上げることのご協力いただきたいと思います。どうかよろしくお願いいたします。
第21回基礎から学ぶ薬剤師塾では直接の質問は残念ながら皆無でしたが、チャットでの質問、アンケートでの質問をいただきましたので、いつものようにQ&A方式で回答させていただきます。
半減期の延長する薬物=初回通過効果は受けなかったけど、全身循環血が肝臓を通るたびに消失の遅延が生じる薬物(肝でのCYP2C9による代謝を腎不全では受けにくいフェキソフェナジン、
などを思い浮かべるとよいですね。Y軸が対数軸だと半減期の延長が明らかにわかりやすくなります。
チャットでの質問
北上済生会病院 八重樫恭平先生
Q.腎保護の観点からRAS阻害薬を使用する場合、半減期が長いものほど有効でしょうか。
A.あまり考えたことがありません。ACE-Iは腎排泄なので、腎機能が低下するほど半減期は長くなります。半減期の長短により腎保護作用が強力かどうかについてはあまり知りませんが、ACE-Iに関しては汎用されているエナラプリルの活性代謝物35hr、リシノプリル34~39hr、ベナゼプリルの活性代謝物22hrと長いものが多いです。ARBに関してはバルサルタン4~6hr、ロサルタン活性代謝物4hr以外は10hr以上ですが、半減期の長いものの効果が高いとは思えません。RAS阻害薬同士の直接対決のRCTでもやらない限り、どちらが有効かを証明することはできないと思いますが、おそらくやられていないと思います。RAS阻害薬はクラスイフェクトとしてタンパク尿・アルブミン尿のある患者の腎保護を期待できますので、RAS阻害薬を投与するうえではタンパク尿・アルブミン尿の有無の方が重要だと思います。
ファーマライズ薬局 羽村知穂先生
Q1.今のトリプルワーミーのNSAIDsについてですが、例えばカロナールなどの腎排泄ではないものに変更をお願いするのがいいのでしょうか。他の痛み止めだと湿布や外用剤などで対応するしかないのでしょうか。
A.痛み止めはほぼすべて肝代謝薬物だと思います。NSAIDsによる腎障害、その他の副作用を回避するために有効で、NSAIDsよりも安全なものといえば、アセトアミノフェン(米国FDAはこれを推奨)、セレコキシブ(他のNSAIDsよりも腎には優しく心血管系に悪影響しないが、FDAは心筋梗塞が多発したロフェコキシブ事件からか、類薬のセレコキシブを推奨していません)、吸収しにくい外用パップ剤、痛みが強ければトラマドールなどが考えられます。あとはプラセボ効果を期待してノイロトロピン(副作用があったと聞いたことがない)、その他の漢方薬まで含めると選択肢はたくさんあります(図)。

Q2.アバスチンを点滴治療している方でたんぱく尿2+が出てきて血圧も上昇してきた場合、腎機能の保護のためにやはりRAS阻害薬がよろしいでしょうか?ファーストチョイスをしてカルシウム拮抗薬の方がいいのでしょうか?
A.抗VEGF抗体のベバシズマブは高血圧・タンパク尿を起こしやすい分子標的薬です。ベバシズマブ投与によってVEGFが阻害される、あるいはVEGFの欠損によって糸球体内皮障害が起こり、タンパク尿・腎機能悪化をきたします。タンパク尿2+であれば、タンパク尿のある患者での第1選択薬である降圧薬のRAS阻害薬を投与すべきと思います。
ココカラファインヘルスケア 恒吉春香先生
Q.心不全症例で、Triple whammy予防のために、利尿薬をループ利尿薬のかわりにSGLT2阻害薬を提案してみてもいいのでしょうか?そのときに押さえるポイントなどがあれば教えて下さい。
A.SGLT2阻害薬の利尿作用は持続しません。カナグリフロジンの尿量増加は1日のみです。その他のSGLT2阻害薬も糖利尿は持続しますが、Na利尿は初期のみで、尿量増加が期待できるのも短期間です。したがってSGLT2阻害薬は利尿薬の代わりにはなりませんが、利尿効果に関してはループ利尿薬と相乗作用を示しますので、ループ利尿薬を減量できるでしょうし、利尿薬による急性腎障害の予防は期待できるかもしれません(ただし投与初期の脱水には要注意!)。ARNIの利尿作用はANP, BNPの利尿作用(血管拡張作用もあります)によるものなので、SGLT2阻害薬よりも長期的な利尿作用は強いので利尿薬や降圧薬を減量できます。
飯塚病院 田先先生
Q.利尿薬によるトリプルワーミーのリスクはループ系とサイアザイド系で差に関する報告などはありますか?
A.トリプルワーミーの原因薬としての利尿薬は一般的には利尿降圧薬(利尿作用のある降圧薬)として投与され続けるサイアザイド系を指しているのだと思います。利尿作用がメインで降圧作用の弱いループ利尿薬は浮腫や心不全の呼吸困難などの症状があるときに短期間使います。半減期が短く降圧作用も弱いため、腎機能が悪化してサイアザイド系が効かない腎不全患者にしか降圧薬として使うことはありません。ループ利尿薬の利尿作用は非常に強力なため、当然、脱水をきたしやすく腎機能悪化リスクは高いとは思いますが、このように使用方法が異なりますし、使用対象患者も異なりますので、AKI発症リスクを比較できないと思います。
みきやま病院 田中先生
Q.体重が30kg程度で、シスタチンによるeGFRが30ml/min台の高齢者に経口抗菌薬を投与する場合、クレアチニンクリアランス30ml/min以上あれば減量の必要なしとなっているものは、減量せず通常投与量を投与した方がよいでしょうか。腎臓に関してアレルギー性の障害が多いなら、セフェム系やペニシリン系は副作用を心配して減量する意味は乏しいでしょうか(本題からやや外れた質問ですいません)
A.感染症は急性疾患ですので、「腎機能が低下していても用量依存的な副作用のないβラクタム系は積極的に投与すべし。初日投与量は腎機能が低下していても常用量投与すべし」というのが持論ではありますが、体重が30kgの高齢者というのであれば、一般成人の1/2の体重と考え、初日投与量は1/2の用量で十分です。その後は使用する抗菌薬の尿中排泄率によって用量・投与間隔を調整します。βラクタム系は安全とは言っても腎機能の低い後期高齢者に常用量で投与し続けるとけいれんなどの中枢症状は起こりえます。
保険薬局の先生方に気を付けていただきたいのはCCr<30で禁忌となっている場合、CCr≧30であればOKと考えCCr31mL/minであれば静観し、CCr29mL/min になれば疑義紹介する「デジタル薬剤師」にならないことです。同様に腎機能別用量がCCr<30で1000mg、CCr≧30の用量が2000mgであった場合であってもCCr29mL/minとCCr31mL/minの腎機能に差があるとは思えませんので、1人1人の患者さんの腎機能の変化、病態の変化を1点のみでとらえるのではなく、間を取って1500mg程度が適切用量だと考えてください。あとは腎機能がよくなりつつあるか、悪くなりつつあるかを観察していただき、そして体格も考慮したうえで用量を決めていただきたいと思います。
I&H株式会社 那須裕之先生
Q.外用ビタミンD3製剤について、①オキサロール以外も腎機能障害のある人に使用しないほうがいいですか?②NSAIDsの代わりにアセトアミノフェンを使うように、何か代用薬はありますか?
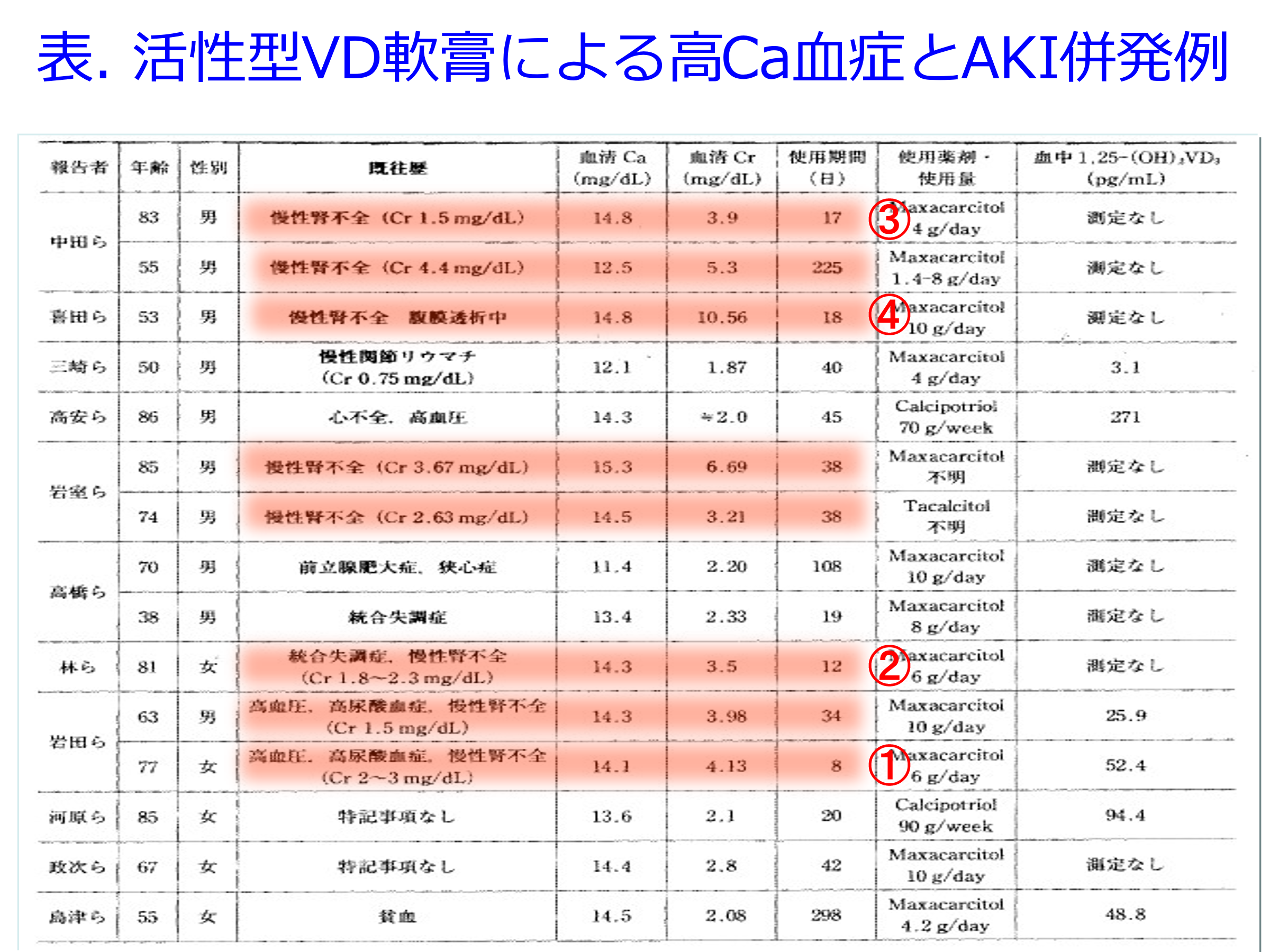
A.添付文書上では腎機能低下患者に外用活性型ビタミンD軟膏の全身塗布は禁忌ではありませんが、お見せしました平山先生の表では(表)、もともと腎機能の低下している症例(赤色)は極めて速やかに腎障害を発症しています(発症順に①②③④で示しています)。血清クレアチニン値は2~4週間に1回測定されると仮定すると①8日目、②12日目、③17日目、④18日目に腎機能が悪化したと考えるよりも、たまたま8日目に測定したから腎機能悪化を発見でしただけで、もっと速やかに腎障害が進行していた可能性は大いにあると考えられます。そのため、腎機能低下患者には外用活性型ビタミンD軟膏を全身塗布すべきではないと思います。ほぼすべての急性腎障害発症のリスク因子で最大のものは「既存の腎機能低下および高齢者」であることを肝に銘じていただきたいと思います。
ステロイド軟膏は抗炎症作用を期待して投与されますが、皮膚委縮や毛細血管拡張、感染症を誘発するとされており、活性型ビタミンD軟膏は強皮細胞の増殖抑制、分化誘導作用を期待して投与されますが、効果発現までに時間がかかると理解していますが、皮膚科で使用する薬剤についてはあまり詳しくないため、活性型ビタミンD軟膏の代用になる薬剤についてはよく知りません。申し訳ありません。
アンケートでの質問
国際医療福祉大学病院 大矢智則先生
Q.答えを聞き漏らしていたら申し訳ありませんが1点ご教示ください。講義の中でエディロールなど活性型VD3製剤の処方について整形外科医に中止を求めるという内容がありました。骨粗鬆症の予防にはエビデンスありませんが治療に対してはガイドラインによる推奨のある中で、薬剤師は骨粗鬆症があっても腎機能障害リスクや潜在的腎障害リスクと判断したら活性型VD3製剤の中止を提案すべきでしょうか?それとも講義中にありました定期的な腎機能モニタリングなどを提案すべきでしょうか?
A.「活性型VD3製剤の処方について整形外科医に中止を求める」とは言っておりません。活性型VD3製剤の添付文書上では定期的な血清Ca濃度のモニタリングが必要なのに、整形外科の先生方は一般的に採血をしていただけないことが多いのです。それによって特に後期高齢女性で高カルシウム血症による多尿・脱水から腎機能低下が起こると一般内科から腎臓内科に紹介入院になることが多いのです。閉経後骨粗鬆症に活性型ビタミンDの投与は必要です。ただし投与後の副作用モニタリングも必要だと言いたかったのです。間違って伝わっているとすれば、ごめんなさい。何も起こっていないのに活性型VD3製剤の処方を整形外科医に中止を求めることはあり得ません。
所属・氏名を記していただいた質問でしたが、厳しめの回答になったため氏名の公表を差し控えさせていただきます。
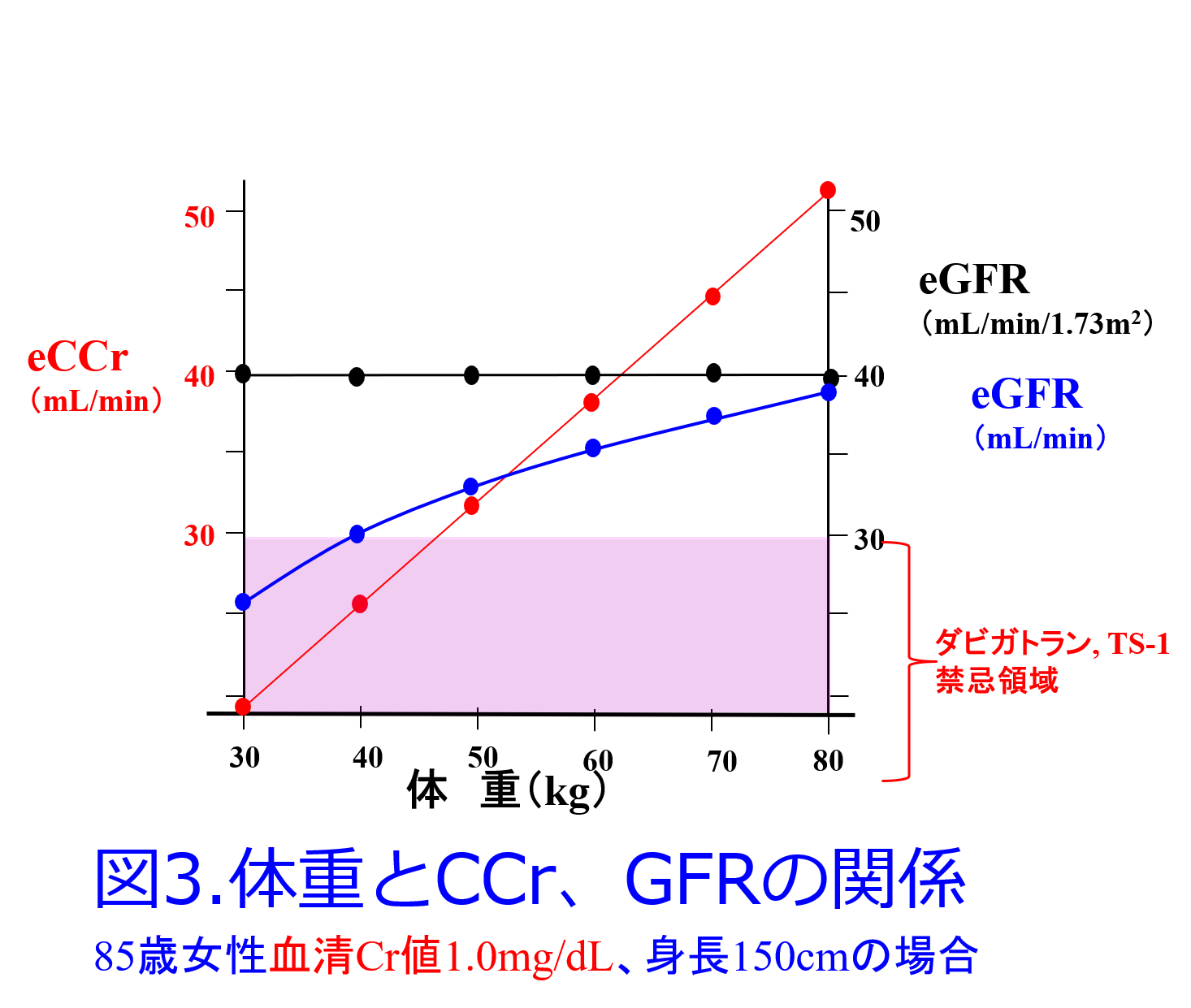
Q.小柄な高齢の女性は急性腎障害に注意とありましたが、日常の投薬設計時に理想体重補正したクレアチニンクリアランスを計算して、禁忌に達していたらDr.に疑義紹介しているのですが、この時に小柄な高齢の女性の患者さんの場合は本当に腎機能が悪いのか、体が小さい(体重補正すると尚一層なのですが)過小評価しているのか判断に迷う時があります。特にDOACなどの止めるのもリスクのある薬の場合判断に迷います。又、体の大きな男性高齢者でも寝たきりの状態であれば、クレアチニン値が低い時は0.6を挿入したりしています。この事について平田先生のご意見をお聞かせ頂けると幸いです。
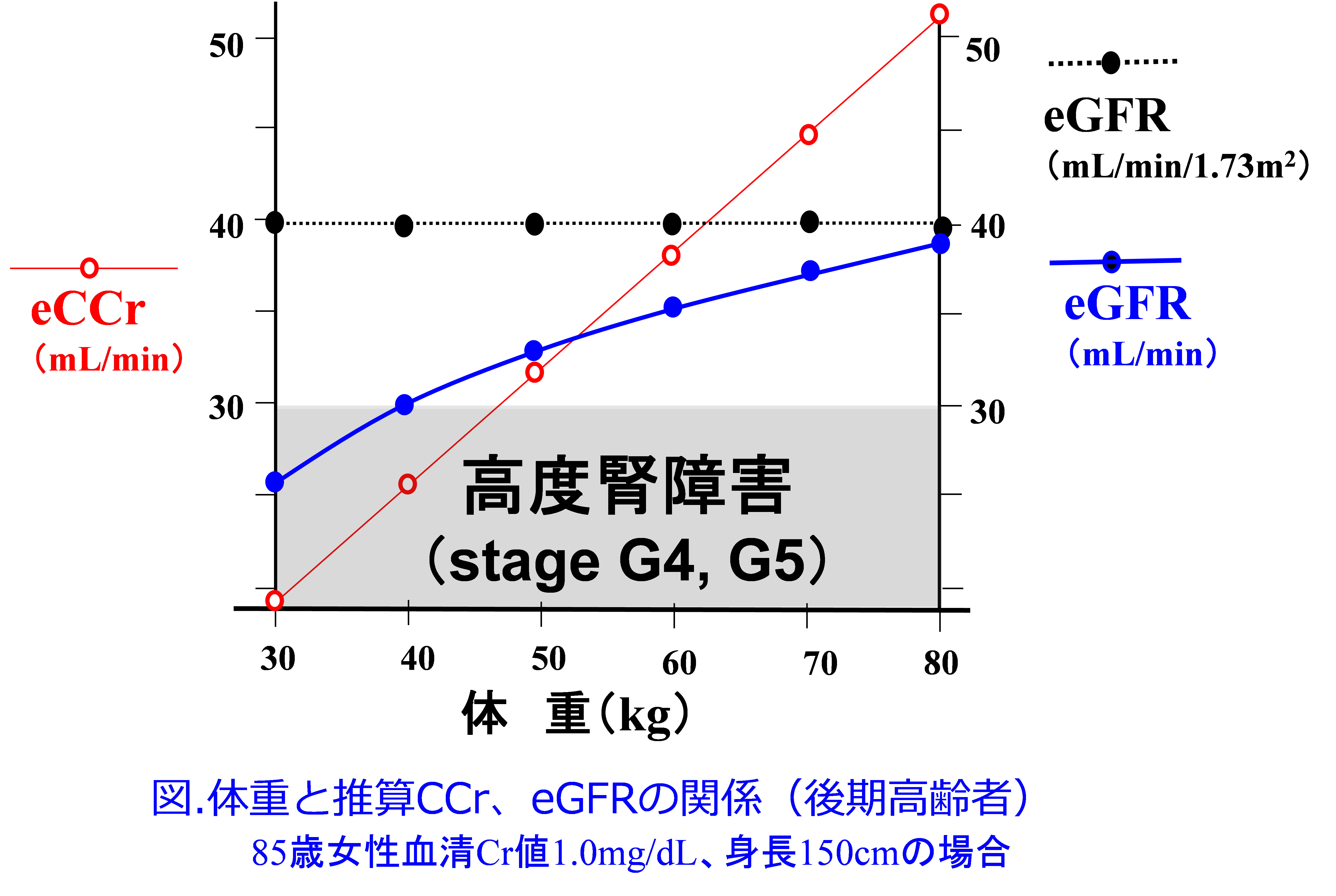
A.クレアチニンクリアランスの推算式(CG式)は加齢に伴い直線的に低下する式なので(図)、フレイルなどの高齢者には過大評価になりがちなeGFRに比べ一般的にフィットしやすいです。CG式で最も考慮すべきポイントは肥満患者で過大評価しやすいことだと思います。その時には理想体重を使うこともありますが、多くの場合は補正体重の方がベターだと思っています。小柄な高齢女性でCG式に理想体重を代入する意義はないと思います。また血清クレアチニン値の代わりに0.6を代入するラウンドアップ法をCG式で使うと、これも腎機能の過小評価になってしまい、薬用量が少なすぎて効かなくなる恐れがあると思います。僕自身は腎機能が評価しにくい痩せて小柄な超高齢者ではeGFRは過大評価されがちなので安全性を考慮してラウンドアップ法を使うのはやむを得ないとは思いますが、CG式のラウンドアップはお勧めしません。
補正体重(Adjusted body weight:補正体重(kg)= 理想体重+[0.4×(実測体重-理想体重)]
これも所属・氏名を記していただいた質問でしたが、厳しめの回答になったため氏名の公表を差し控えさせていただきます。
Q.心不全増悪で入院の80代後半、非透析患者様で、eGFR(Cy)一桁、フロセミド20mg1T/1x、タケルダ、ベラパミル40mg3T/3x、ジャヌビア12.5mgなどを服用中でした。利尿薬調整後に改善し退院が決まった一方血圧は上昇してきたため、中止していた持参薬テルミサルタン20mg2T/2x再開を医師に打診すると、「腎血流量減ってさらに腎機能悪くなるのでは」と。このとき薬剤師としてどうするべきだったか考えています。例えばガイドラインで推奨される薬剤でも、弱った高齢者に追加することでdouble whammyによる腎機能低下が危惧されるジレンマに遭遇したとき、薬剤選択について指針となる考え方はございますでしょうか?
利尿薬やNSAIDsの併用がなければ、弱った高齢者でもACE阻害薬/ARBの腎保護作用は期待できると考えてよいですか?お忙しいところ恐縮ですが、ご教授頂けますと幸いです。
A.eGFR(Cy)一桁ということは末期腎不全で透析導入間近の症例ですね。RAS阻害薬を持続すると糸球体過剰濾過を抑制して、透析導入が早まることを懸念して主治医はテルミサルタンを中止したのではないかと思います。RAS阻害薬は蛋白尿・アルブミン尿のある患者、慢性心不全患者では非常に頼りになる薬ですが、一方で、腎機能が悪化し高カリウム血症を起こしやすい降圧薬です。そういうリスクの高い患者さん(特に腎機能の低下した後期高齢者)で降圧薬が必要であれば、腎虚血による悪影響を及ぼさないCa拮抗薬の方が、使いやすいと思います。
第20回 基礎から学ぶ薬剤師塾 Q&A
第 20回 基礎から学ぶ薬剤師塾 Q&A
腎機能低下時に減量が必要な薬
~根拠は尿中排泄率だけじゃない~
前回の基礎から学ぶ薬剤師塾「腎機能低下時に減量が必要な薬~根拠は尿中排泄率だけじゃない~」はむつかしかったというアンケート結果が多かったです。おそらく前半はいつも話している腎排泄性薬物による副作用なので優しかったのでしょうが、非腎クリアランスの低下する薬は「このCYPが問題!このトランスポータが問題だ!」などと言い切ることができないため、まとめにくい内容です。それでもCYP2C9基質は腎不全・尿毒素の影響を受けやすいということがある程度、予測できるようになったことを中心にまとめさせていただきました。
バイオアベイラビリティが低下する薬物、半減期の延長する薬物も難しかったかも?
バイオアベイラビリティが低下する薬物=小腸における初回通過効果(CYP3A4)を受けにくいか、肝における初回使用効果を受けにくい薬物=投与量を増やしたのと同じ
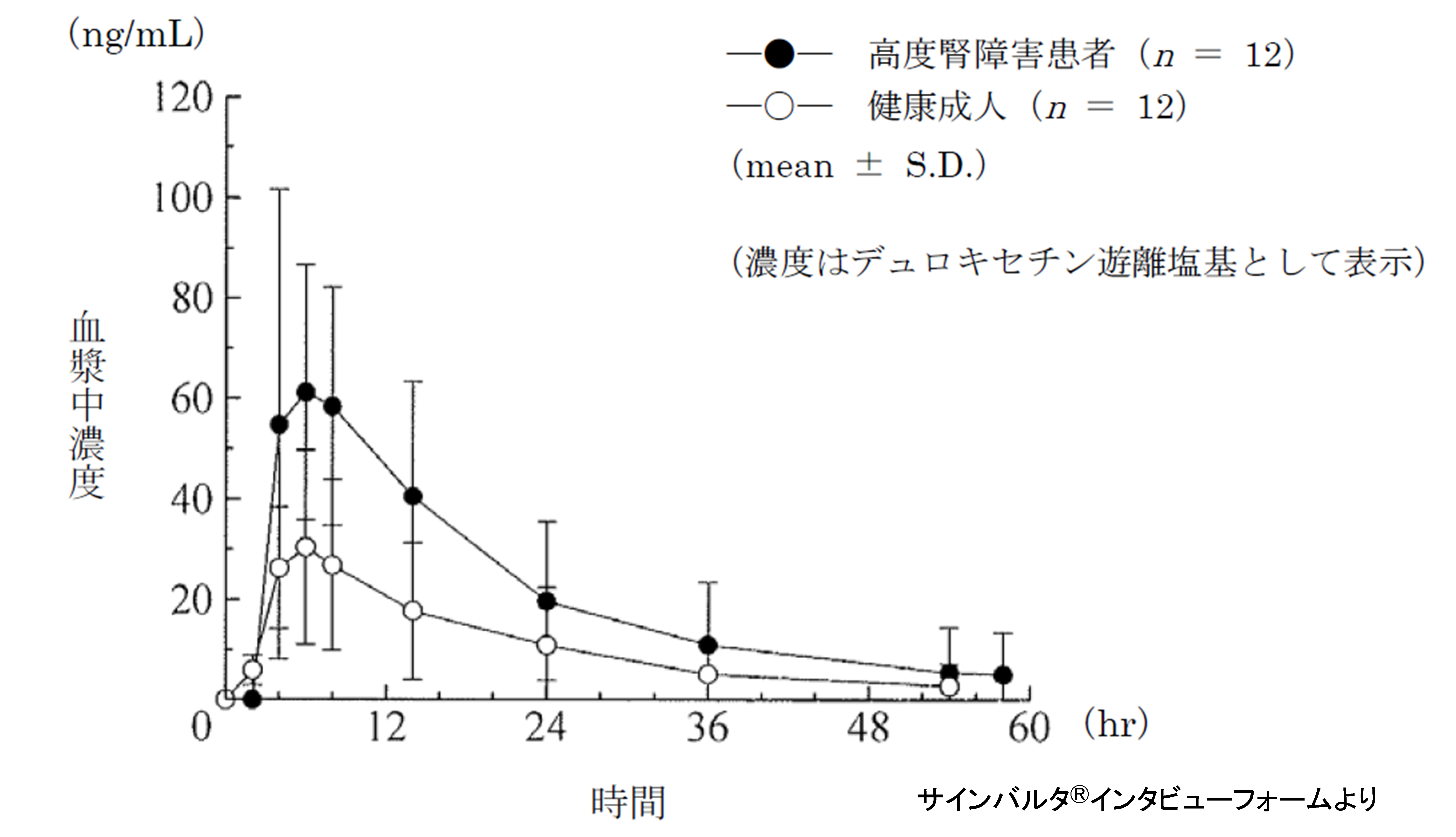
半減期の延長する薬物=初回通過効果は受けなかったけど、全身循環血が肝臓を通るたびに消失の遅延が生じる薬物(肝でのCYP2C9による代謝を腎不全では受けにくいフェキソフェナジン、
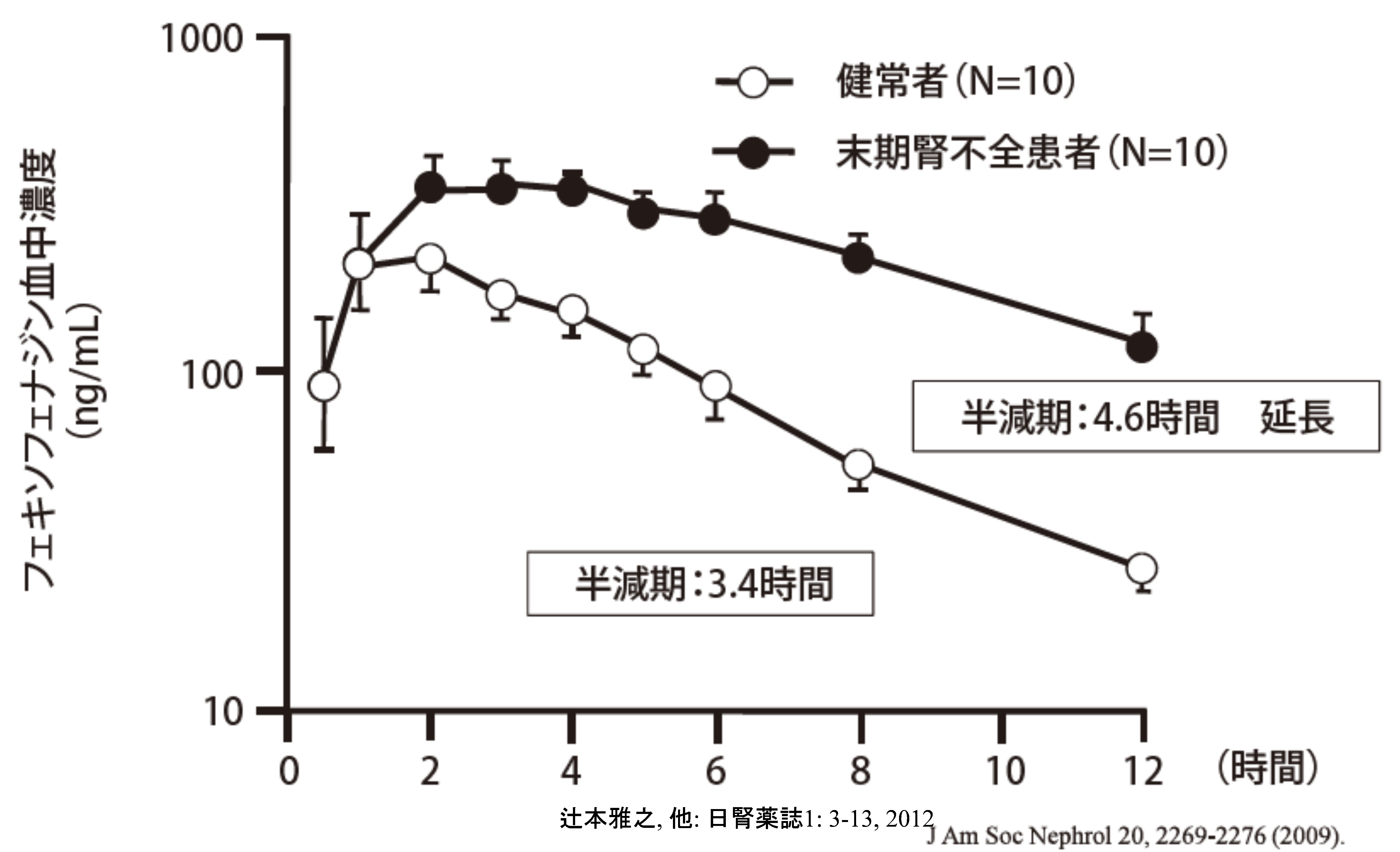
肝臓に取り込むOATPが腎不全では機能しないため肝代謝が遅延するエリスロマイシン)
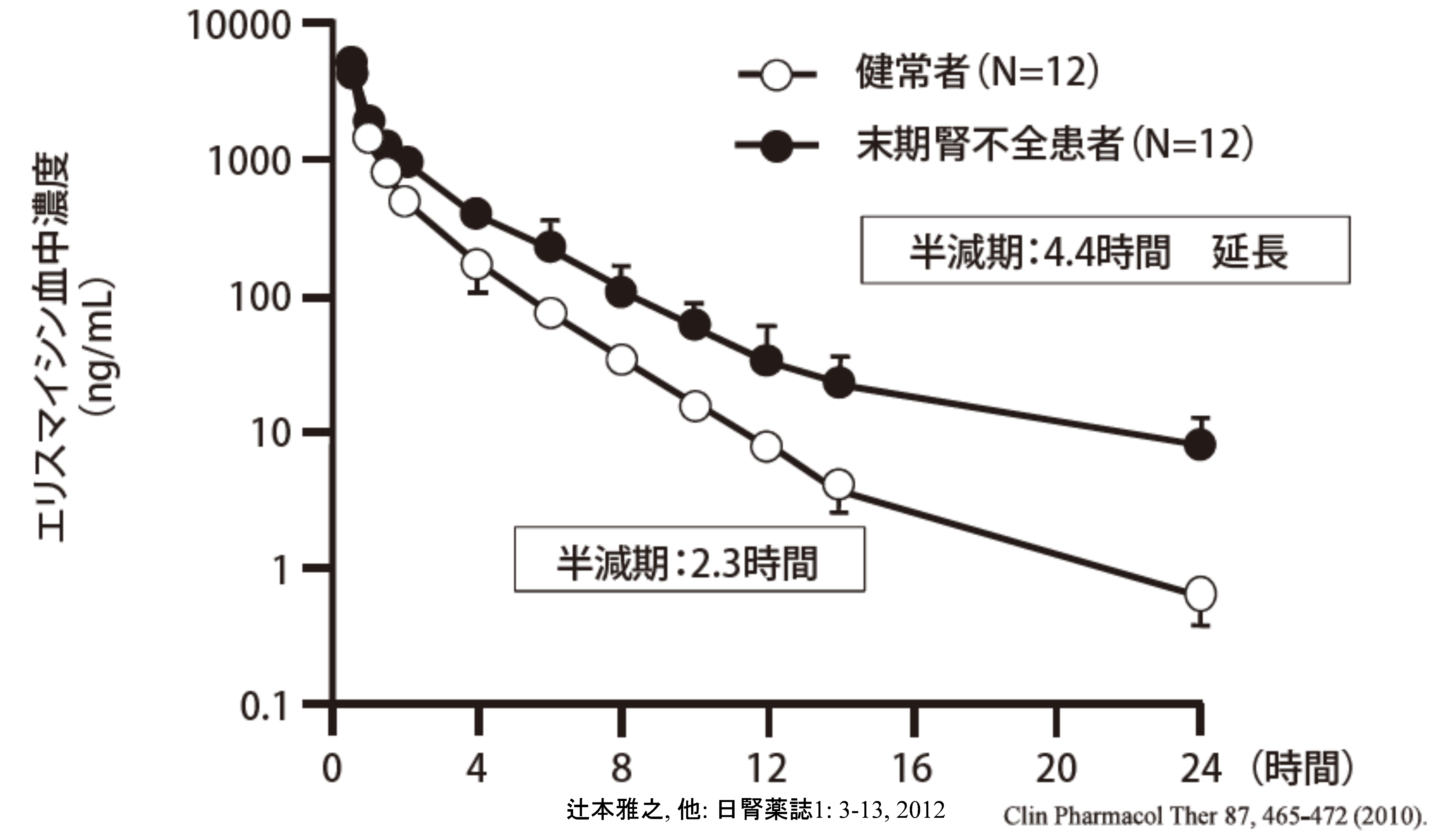
などを思い浮かべるとよいですね。Y軸が対数軸だと半減期の延長が明らかにわかりやすくなります。
講演後のアンケートでいただいた質問
ファーマライズ薬局株式会社 羽村知穂先生
Q1.内容としてとても面白かったのですが、やはり難しく感じました。薬物の中で腎排泄のものが肝代謝より少ないので腎を覚えてというのはとても参考になりました。ただ覚えることが多いのでまずは代表的な薬品の尿中排泄率を覚えていくのがいいのでしょうか?
ただ肝臓で代謝された活性代謝物も腎排泄として腎機能低下している方は蓄積により副作用の上昇を考えなければならないというところでまずは高齢で小柄の方、腎機能低下がある人は注意という着眼点でいくのがいいのでしょうか?
A.リスクの高い腎排泄性薬物を覚えてゆけばよいでしょう。日本腎臓病薬物療法学会(JSNP)では学会HPに「腎機能低下時に最も注意が必要な薬剤投与量一覧」を掲載していますが、これだけでも236薬品あります。じほうから発売されている腎機能別薬剤投与量 pocket book 第4版または学会HPで会員のみが閲覧可能な「腎機能別薬剤投与量一覧」では◎になっているものが最重要となりますが、これは「腎機能低下時に最も注意が必要な薬剤投与量一覧」に載っているものはすべて◎です。236薬品ってすごく多いですが、同一薬効でヨード造影剤やアミノグリコシド系抗菌薬など薬効を基準に見てみると意外と共通点があります。ポケットブックでは次に重要な薬物は〇、気を付けていただきたいものは△にしていますので、この順に重要と考えていただくとよいでしょう。腎排泄性ではなくても活性代謝物が蓄積しやすいハイリスク薬物のSU薬も◎にしていますが、グリクラジド(グリミクロン)は〇です。
そして副作用のターゲットになりやすいのは体格・腎機能が小さいのにそのどちらか、あるいは両方を考慮せずに投与してしまった場合が最も起こりやすいです。それが「小柄な後期高齢女性」です。講義でも説明したとおり、プレガバリンもバラシクロビルもシベンゾリンも小柄な後期高齢者で副作用が頻発していいますから。
Q2.グリーンブック並びにポケットブックは、2024年の9月までに入会すればもらえるとおっしゃっておりましたが、今年入会しても来年になるという認識でよろしいのでしょうか?
A.JSNPの会計年度が8月31日ですから、2022年8月31日までに入会していた方には4月頃にグリーンブック、9月頃にポケットブックが郵送されました。2023年の作成予定はありませんので、2024年の8月末までに会員になっていれば(必ずしも2023年8月末に会員でなくても)、グリーンブック(特別号改訂5版)並びに新規改訂版の腎機能別薬剤投与量 POCKET BOOK 第5版がもらえます。
I&H 運営管理課 那須裕之先生
Q.プレガバリンを腎機能の低下した患者に投与する際、添付文書の表記に従うと過量になるリスクがあることをご解説いただきました。ミロガバリンはいかがでしょうか?ミロガバリンについても添付文書に記載があります
A.申し訳ありません。医中誌およびPubMedで比較しようとしましたが、ミロガバリンは米国では発売されていないようで情報が不足しており、私自身も経験がありませんので、全くわかりません。
そのほかにも質問がありましたが、ご質問される場合には、所属と氏名のご記入をお願い致しておりますので、所属・氏名が不明な場合は、お答えできません。今回は講演後の質問はありませんでしたが、薬剤師塾の理想は氏名・所属を明らかにしたうえでのディスカッションを目指していますので、よろしくお願いいたします。
平田への講演依頼に関しましては平田のメールアドレス
hirata@kumamoto-u.ac.jp までお気軽にご連絡ください。
第19回 基礎から学ぶ薬剤師塾 Q&A
第 19回 基礎から学ぶ薬剤師塾 Q&A
腎機能悪化を防ぐこれからのtriple therapy
~SGLT2阻害薬、ARNI、MRAの適正使用について考える~
講演中にいただいた質問
I&H株式会社 那須裕之先生
Q1.心不全患者にSGLT2阻害薬を投与する際の「こまめな飲水」は具体的には何時間おきにすればいいのですか?
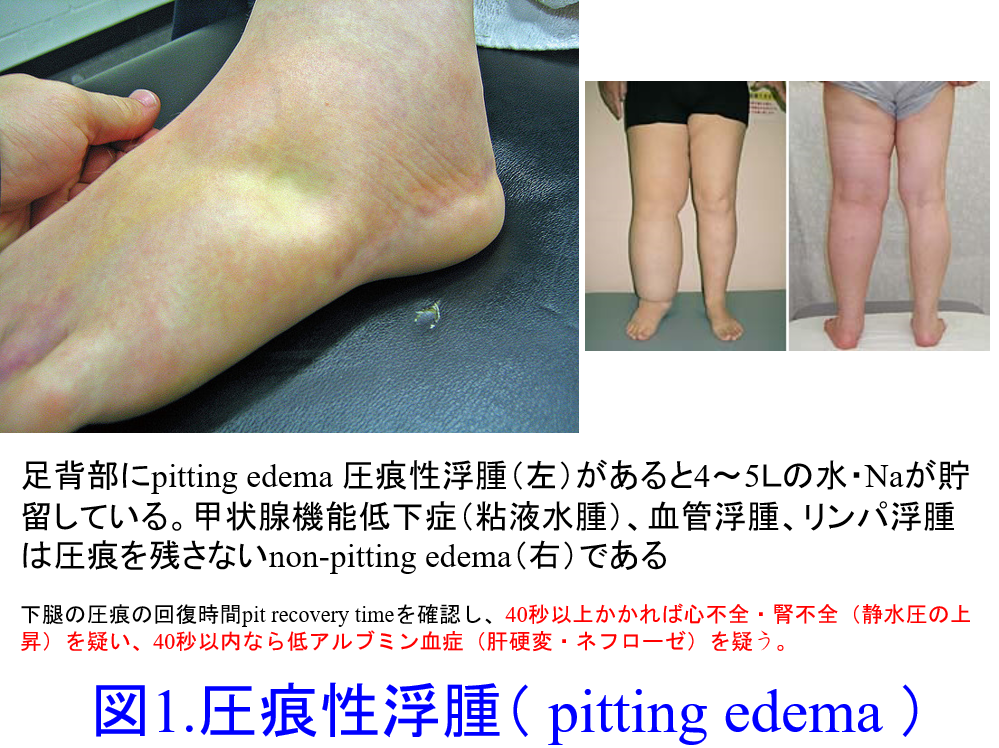
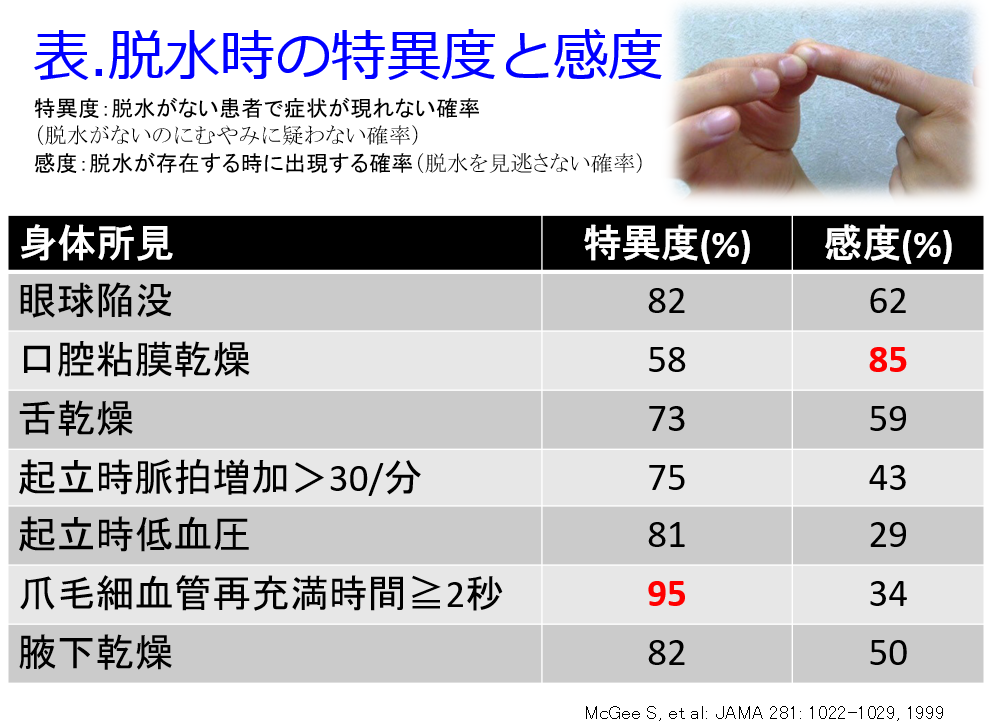
A.重症の心不全では心不全患者の心不全悪化による入院理由で溢水による呼吸困難などはよくあることで、ループ利尿薬を投与して症状が軽減したら退院します。このような症例に対して、飲水励行はしません。ただし心不全患者の多くが高齢者(口渇中枢の機能が低下している)であることを考慮すると、飲水量は少なめであっても「こまめな飲水」をしてもらわないと、SGLT2阻害薬の副作用である脱水(とそれに伴う腎機能悪化)、性器感染症、糖尿病性ケトアシドーシスになりやすくなりますので、医師の指示した1日飲水量、例えば冬では1日1.2L程度、発汗の多い夏にはより多め水をのどが乾いていなくても少量ずつ飲んでいただくことになります。具体的に1~2時間おきでしょうか。起床時やお風呂上がりにも飲んでいただきましょう。むくみ(足背部の圧痕性浮腫pitting edema:図1)、体重増加、息苦しさがあれば飲水量を少なめに、逆に脱水(皮膚の張り:図2、口腔内乾燥のチェック、爪毛細血管再充満時間≧2秒(表)など)、体重減少などがあれば多めの飲水を心がけてもらってもよいでしょう。

Q2.SGLT2阻害薬による尿糖排泄作用はずっと持続するはずなのに、カナグルⓇの利尿作用は1日のみなのはなぜですか?
A.SGLT2阻害薬後の尿量変化の報告が少ないので、明確ではないのですが、カナグルⓇに関しては初日にプラセボに比し、尿量の増加が認められましたが、この効果は2日目以降には消失したと報告されており1)、カナグリフロジン、ダパグリフロジン、エンパグリフロジンともに投与1日目には尿量が増加するものの、7日目には投与前と同じになる(7日以内に利尿が消失しているのは確かだがいつ利尿作用が消失したかは不明)という報告もあります2)。ダパグリフロジン投与後尿中グルコース排泄量は1週間かけて有意に増加し、尿量は、尿中Na排泄量、尿中Cl排泄量は0日目に比し、2日目に増加したものの、7日目には元に戻った3)。ダパグリフロジン投与後の尿量は7日間にわたり数値的に増加した4)など、報告によって異なります。一方、エンパグリフロジン投与後、800~900mL/日の増加5)がみられた、あるいはエンパグリフロジンの利尿はフロセミド併用によって6週間後も続く6)ことが報告されていますが、これらはいずれもループ利尿薬が併用されています。ループ利尿薬との併用効果は尿中Na排泄量の増加を伴わずに24時間尿量を有意に増加させたことが報告されており6)7)、SGLT2阻害薬とループ利尿薬の併用時の尿中Na排泄分画(FENa)の増強は、単剤投与時に比べて4倍以上であったことも報告されていることから、SGLT2阻害薬とループ利尿薬は相乗作用を示すと考えられ6)、SGLT2阻害薬投与初期及びループ利尿薬併用時には脱水に要注意と思われます。ということでSGLT2阻害薬の利尿作用、Na排泄作用は一過性であるが、薬によってその持続時間は異なるかもしれません。ただしSGLT2阻害薬投与後の尿糖排泄促進作用は持続します。Na利尿は投与初期には認められますが、早期に減弱します。例えばエンパグリフロジン、ダパグリフロジンのNa排泄促進作用は3日以内6)、7日以内には消失します3)。
まとめますと投与2日を超えると7日目でほぼ利尿作用がなくなるという報告もあれば、1か月くらい利尿作用が続く症例もあるようです。概してSGLT2阻害薬投与初期にみられた尿量増加は、持続的にはみられないことが多く、SGLT2阻害薬投与時の尿量は飲水量が規定因子となるため、飲水量や回数を過度に増やすことは頻尿や尿量増加につながります。脱水の副作用は8つのRCTのメタ解析で8)、SGLT2阻害薬群で有意となった副作用の1つであり、発症率も高いため、利尿作用がどれくらい持続するかは重要な問題ですが、今のところ尿量の持続に関する報告は限られています。
SGLT2阻害薬の利尿作用が持続しないメカニズムについては動物実験ではありますが、髄質の尿素増加9)とアクアポリン210)およびバソプレシンV2受容体のタンパク質発現量が増加11)してバソプレシンを介した水再吸収によって、SGLT2阻害薬を継続投与すると、その利尿作用は持続しないと考えられています。Na利尿に関しても近位尿細管でSGLT2阻害薬がNaの再吸収を阻害しても、遠位部でNaを再吸収して低ナトリウム血症になるのを防いでいるのだと思われます。ただしブドウ糖については近位尿細管以外に再吸収部位がないため、糖利尿は持続するのだと思います。
引用文献
1)Tanaka H, et al,: Adv Ther 2017; 34: 436-51
2)Nakagaito M, et al: Circ Rep 2019;1:405-413
3)Masuda T, et al: POJ Diabetes Obes 1: 1-8, 2017
4)Ohara K, et al: Nephrology. 2019 ;24:904-911.
5)Damman K, et al: Eur J Heart Fail. 2020 Apr;22(4):713-722. doi: 10.1002/ejhf.1713.
6)Mordi M, et al: Circulation 2020; 142:1713-1724.
7)Damman K, et al: Eur J Heart Fail. 2020 Apr;22(4):713-722. doi: 10.1002/ejhf.1713.
8)Qui M, et al: Diab Vasc Res Mar-Apr 2021;18(2):doi: 10.1177/14791641211011016.
9)Marton A, et al: Nat Rev Nephrol 17: 65–77
10)Chung S., et al: Front Physiol 10, 271. 10.3389/fphys.2019.00271
11)Masuda T, et al: Physiol Rep 8 , e14360. 10.14814/phy2.14360
沼津市民病院 平野雄一先生
Q.フィネレノン投与時に注意すべき点は?
A.フィネレノンはMRAの中では高カリウム血症を最も起こしにくいと言われていますが、やはりMRAなので、高カリウム血症です。投与初期の腎機能悪化initial dippingはSGLT2阻害薬と比べると非常に軽度ですし、降圧作用・利尿作用も弱いので、ARNIのように過降圧や利尿作用による脱水もあまり問題にはなりません。
講演後のアンケートでいただいた質問
平成横浜病院 廣瀬里美子先生
Q.CKD以外の腎機能の低くなりつつある人たちにもSGLT-2阻害薬は効果があるのであれば、日常症状を感じないのに健康診断で腎機能があまりよくない予備軍の人たちは受診して服薬していくという未来もあるのでしょうか。これで日本の、医療や世界の医療費が軽減するなんて感動します。
A.SGLT2阻害薬は蛋白尿またはアルブミン尿があって腎機能が低下した症例で、腎保護作用が非常に強力になるとされますので、それのない疾患、つまり高血圧が持続すれば腎機能が低下しますが、そのような腎硬化症予備軍が加齢に伴いCKDになっても大きな効果を示しにくいかもしれません。ただしSGLT2阻害薬は長寿遺伝子を活性化させる作用や酸化ストレスを軽減し抗炎症作用を持つなど、腎疾患、心疾患を持たない方にとっても様々な健康増進作用が期待できるかもしれません。
北見赤十字病院 加藤理愛先生
Q.ARNIの腎保護効果はアルブミン尿と関係しないのはなぜでしょうか?
A.Voors AA, et al: Eur J Heart Fail 2015; 17: 510-517の結果に基づいて、36週間後のARNI群の腎機能悪化は-1.5mL/min/1.73m2、バルサルタン群は-5.2mL/min/1.73m2でARNIの方が有意に腎機能悪化速度が緩やかでした(調整後のP = 0.002:図1)が、ARNIの尿中アルブミン/Cr比の幾何平均値はARNI群で増加した(2.1-4.0mg/mmol)のに対し、バルサルタン群では横ばいに推移した(1.5-2.6mg/mmol、36週間の差に関するP=0.016:図2)で2つの介入群間でUACRに有意差が生じました。これって2.1-4.0mg/mmolは18.6-35.4mg/gCrにあたり、1.5-2.6mg/mmol は13.3-23mg/gCrにあたります。尿中アルブミンは30mg/gCr未満は正常ですので、ARNI群はバルサルタン群に比し有意にアルブミン尿を増やしたのは確かですが、単位に騙されました。アルブミン尿はARNIを投与しても平均値としては正常域内です。大変失礼いたしました。図2は意味ないですね。

北九州宗像中央病院 高田由美子先生
Q.eGFRが30前後でHbA1cは6.7前後、ジャヌビアⓇを50mg服用中です。このままで続けるか、SGLT -2を追加するか、SGLT-2に変更するか、処方提案をどうしたらいいか悩んでいます。先生はいかがお考えですか?
A.この症例の年齢、BMIが知りたいです。後期高齢者でBMIの低い症例には使いにくいと思います。
それとSGLT2阻害薬はeGFRが25mL/min/1.73m2未満の患者では、効果が期待できるかどうかについてもよくわかっておりませんし、フィネレノンも高カリウム血症のリスクがあるため、eGFRが30前後の症例に積極的な処方提案はしにくいと思います。
アスヤクlife研修会 Q&A
2022年10月24日 アスヤクlife研修会 Q&A
今回、私の声が聞きにくかったというアンケート結果が多かったようですが、これは私のテンションが低かったからではなく、おそらく機器上の問題だと思います。音が小さいということが早めに分かっていれば、ヘッドセットを交換してみるなどの手段が取れますので、今後はチャットなどを利用して指摘していただければ幸いです。
Q.リオナで、便が鉄臭く、便器にもつくので飲みたくない患者さんが数名いましたが、リオナはタール便ではないのですか?
A.鉄剤による便はタール便ではなく、黒色便です。タール便と黒色便との違いは講演中に述べた通りです。鉄を含む薬剤(特にピートルⓇ)では下痢しやすくなりますし、鉄臭い便が排泄されることはありますが、タール便は消化管出血によるものなので、血液を大量に含み、もっともっと鉄臭く、気色悪いです。
Q.カルタンを服用中にPPIが追加処方された場合、P値に影響がなければそのままカルタンを継続が通常ということでしょうか。それとも念のため他のリン吸着薬に変更していくのでしょうか。
A.カルタンⓇを投与しているのは、低カルシウム血症で高リン血症などのそれなりの理由があると思われます。私の経験ではカルタンⓇ投与中に著明にリンが上がる方はそんなに多くはありません。そのようにリンの上がりやすい方には他のリン吸着薬に変更していただき、血清Ca濃度を上げる必要があるなら活性型ビタミンDの増量などの工夫が必要と思います。
Q.リンを健常者並みにコントロールした方が予後が良いという報告も見かけましたが、先生はどの様に考えますか。
A.私もリンを健常者並みにコントロールした方が予後が良くなると思っています。食事が十分摂れないためにリンが低い方はやせて栄養状態が不良なため、アルブミン濃度も低下し免疫能も低下しますので、感染症などによる死亡率が高くなります。そのため総合的なデータでみるとリンの低い人は死亡率が高くなります。ただしもしも十分な栄養をしっかり摂れている人であれば、3.5~5.0mg/dL程度の低い方がいいです。低すぎはよくありません。
Q.リン吸着力が強い薬剤がたくさん出てきているのに、レナジェルやキックリンの10錠以上/回を選択する理由にどんなことが考えられますか。
A.それは患者さんが下痢気味なのでこれらのポリマーを選ばれたのか、医師の好みか、患者さんの好みかによると思います。鉄が充足していて(フェリチン<300ng/mL)、リオナⓇ、ピートルⓇが投与できない、ホスレノールⓇはむかつきがあるため服用できないなどの問題があるのかもしれません。
Q.腎機能CCrが40台 70代高齢の患者様で徐々に腎機能低下しているのですが、便秘の症状があり酸化マグネシウムが1日3回でよく効いていたのですがどの程度腎機能が下がったら他の薬剤に切り替えるのがいいのでしょうか?血清マグネシウム値などを見ながら考えればよろしいのでしょうか?
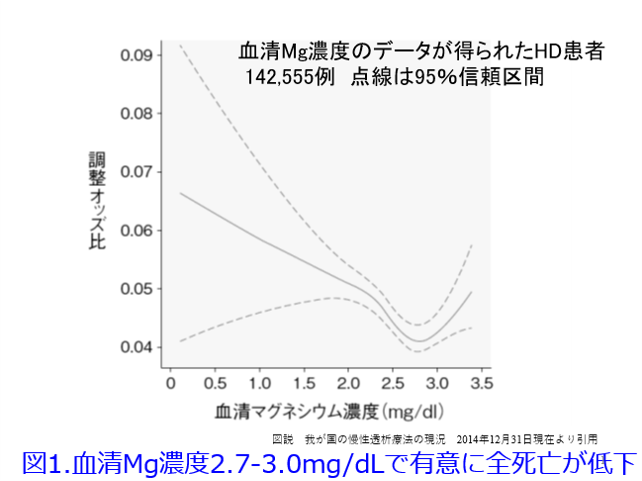
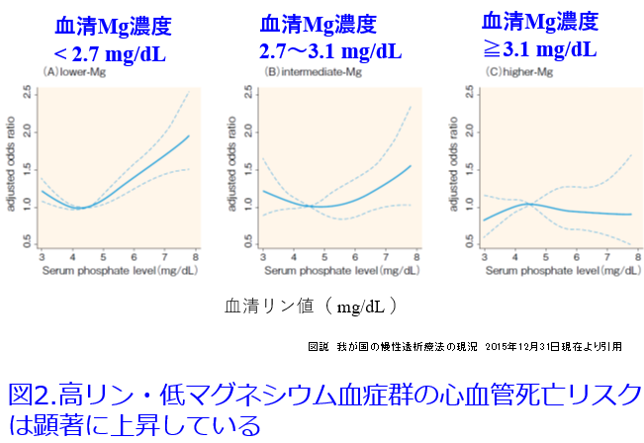
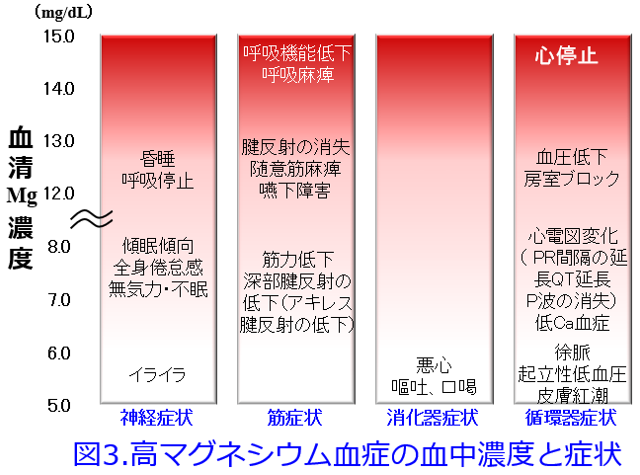
A.血清マグネシウム値をモニターしながらなら、酸化マグネシウムは腎不全患者さんにでも透析患者さんになってでも使えます。ただしさすがに3~6g/日の大量を処方する医師はいないはずです。血清Mg濃度の基準値は1.8~2.6mg/dLとなっていますので、2.6mg/dLを超えると「高マグネシウム血症」と決めつけてはいけません。透析患者の血清Mg濃度は2.7-3.0mg/dLで有意に全死亡が低下したという報告(図1)1)、高リン血症に伴う心血管死亡リスクの上昇は、血中Mg濃度の低い群(血清Mg濃度<2.7mg/dL)では顕著であったが、血中Mg濃度が高くなるにつれてリスクは軽減され、特に血中Mg濃度高値群(血清Mg濃度≧3.1mg/dL)では血中リン濃度が上昇しても死亡リスクは有意な変化を示さなかった(図2)という報告があります2)。さらに血清Mg濃度が低いほどインスリン抵抗性が大きくなることも報告されています3)。Mgは心血管病変を防ぐために重要な元素なのです。ただし定期的なモニターをしていない施設では高マグネシウム血症(図3)を避けるため、腎機能低下患者にMg剤を漫然と投与すべきではありません。
引用文献
1)図説 我が国の慢性透析療法の現況 2014年12月31日現在
2)図説 我が国の慢性透析療法の現況 2015年12月31日現在
3)Chutia H, Lynrah KG: J Lab Physicians 7:75-78, 2015
群馬腎薬「CKD患者さんの療養指導」 Q&A
10月18日に開催された群馬腎薬「CKD患者さんの療養指導~透析導入を減らすための薬剤師からの処方提案~」では質疑応答の時間が取れなかったために、ブログ上で質問に答えさせていただきます。
Q.急性腎不全患者で入院した患者の内服薬について。薬の用量の考え方が難しいです。3剤ほど減量の提案をしたのですが「元々の腎機能は正常な患者なので問題ありません」との回答でした。
A.急性腎不全というのは急性腎障害(AKI)の中でも重篤なものとして考えると、急性腎不全時によって腎機能が急激に低下して一時無尿になったとしても、血清クレアチニン(Cr)値はすぐに下がってくれないことがあるため、急性腎不全時発症直後の腎機能の評価はむつかしいです。通常は血清Cr値によるeGFRでは腎機能が過小評価されますので、腎排泄性薬物の過剰投与が危惧されます(図)。
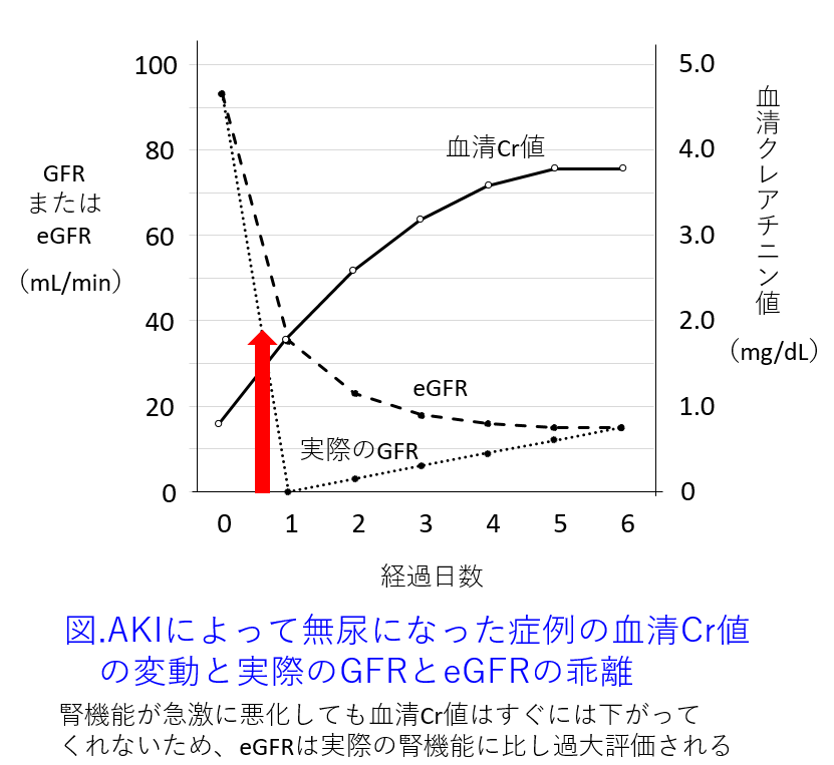
ただし脱水などによっておこる軽度の腎障害の場合、医師の判断では急性腎障害になったけれど回復しつつあるという判断をされたのかもしれません。たとえば、いつものCCrは50以上だったけど、今回だけ、明らかな脱水によるAKIで一時的にCCr<30になっただけなのに「メトホルミンは禁忌ですので中止してください」という疑義照会をしたら、医師から怒られたという話をよく聞きます。病態を十分、観察して検査値の動きを把握しておけばこのようなことは起こらないですね。
例えばSGLT2阻害薬を投与されている患者の腎機能が今回だけ下がっても、副作用が起こるわけではなく「効きにくくなる可能性がある」だけですから、疑義照会は熟慮してやりましょう。CCr<30で禁忌の薬があった時、29になったという1回の検査値のみで疑義照会をする「デジタル薬剤師」にならないよう注意したいものです。
Q.血圧を下げすぎるとeGFRが下がるとのことですが、降圧薬の服用をしていない低血圧の体質のCKD患者さんは血圧を100/50くらいにあげた方がいいのでしょうか。
A.血圧を下げすぎると当たり前にeGFRが下がるのではなく、正確にはSPRINT studyで収縮期血圧を120mmmHg以下に下げた群でeGFRが低下した症例が有意に多かったということです。血圧を下げすぎるとみんなeGFRが下がるわけではありません。
高血圧を放置すると腎硬化症によって高齢者になると腎機能が悪化することはふつうにあります。ただしこの状況を通り過ぎて、さらに高齢になると心機能が低下して血圧を上げることができなくなって腎血流が低下します。心腎連関といいますね。このような状態であれば動脈硬化は進行していて収縮期血圧は高いものの、拡張期血圧が低い、つまり脈圧が大きくなります。収縮期血圧が高いので、血圧を下げたいのですが、拡張期血圧が低すぎて降圧薬を使いにくくなります。
低血圧は低血圧症状のある人に対しては治療が必要ですが、無症状の人であれば治療する必要はありません。駆出率の低い心不全になったために血圧が下がった(血圧を上げる力がなくなった)症例に、RAS阻害薬やβ遮断薬を投与すべきかとなると、非常に悩ましいと思います。循環器医のご判断にお任せするしかないと思います。
Q.アセトアミノフェン750〜1000mg/回を推奨というお話がありましたが、これは体重50kg程度として考えてよろしいでしょうか。
A.体重50kg以上として考えてください。80歳以上の高齢女性で35kgなんて症例では500mgでも十分だと思います。
Q.心不全治療でfantastic fourとして注目されているARNIですが、RAS阻害薬に比較して腎障害作用が少ないとの一部データもあるようです。平田先生の見解はいかがでしょうか。
A.ARNIに関しては今のところ心不全に対する報告のみで、そのサブ解析でARNIのCKD予防作用はSGLT2阻害薬単独よりも明らかになっています血清クレアチニンの0.3 mg/dLを超える増加(AKI)および/またはeGFRの25%以上の低下,ESRDの発症,または腎死の複合アウトカムではARNIはRAS阻害薬群に比し、有意に優れていました(RR 0.84; 95% CI 0.72-0.96, p = 0.01;図)。
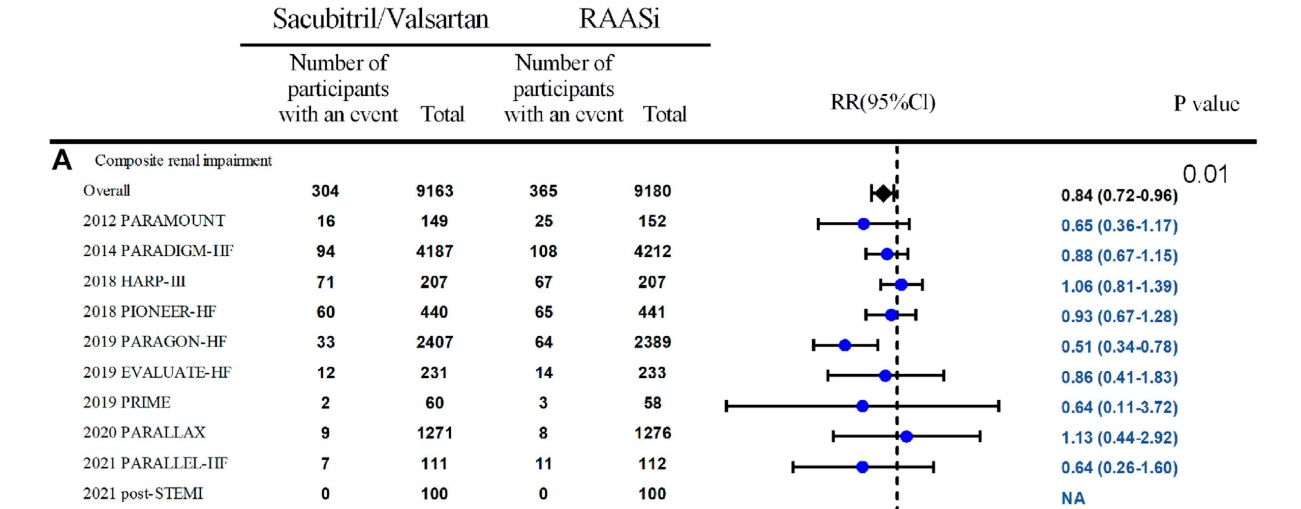
しかし降圧作用がARNI>RAS阻害薬だし、ARNIはANPやBNPを産生させるため利尿作用も強いことから、AKIには要注意かもしれません。上記のデータはあくまで複合アウトカムですので。カリウムの上昇はRAS阻害薬よりもやや軽度みたいです。
引用文献: Xu Y,et al. Front Pharmacol 2021 Nov 19;12:604017.
Q.トリプルワーミーを見た瞬間に疑義紹介するべきですか?
A.弱った高齢者のトリプルワーミー処方に関しては疑義照会すべきです。ただし、ちゃんと理論武装して、資料を見せて、医師に納得してもらわないと、その後のトリプルワーミー処方の減少にはつながらないと思います。ぼくが保険薬局薬剤師だったら電話で疑義紹介した後、論文を持参して医師とディスカッションしに行きます。
Q.米国と日本のCVDリスクと透析導入の差については医療制度の違いなどが影響しているのでしょうか?
A.アジア人はインスリン分泌量が少ないので、太りにくい。そして米国での食事摂取量や摂取カロリー量ははとても多いので肥満患者が非常に多いです。米国では心筋梗塞・心不全による死亡ががんよりも高いのは肥満が最も心血管病変リスクになっているためと思っています。貧しい人ほど安価なファストフードを食べざるを得ないので貧困者の方が肥満になりやすく、貧しいがゆえに保険を持っていない事によって心血管病変を起こしても十分なケアができないこともその理由だと思います。米国の医療レベルは非常に高いものの、先進国の中で皆保険制度がない国は米国だけといわれていますので、米国人のCVDリスクが高いのはおっしゃる通り医療制度も関与していると思われます。
Q.エンパグリフロジン開始初期はeGFR低下前か低下後、どちらの値で腎機能評価を行うほうが良いのでしょうか?
A.SGLT2阻害薬の投与によって腎機能は少しだけ低下しますが(効きすぎると腎機能が悪くなりすぎて投与しにくい人もいますが・・・)、過大評価も過小評価もされていないのですから低下後、その時の腎機能をそのまま用いるべきだと思います。
Q.腎保護作用についてはナトリウム利尿との認識でしたが、スライドの中でATPの消費量が影響しているのでしょうか?
A.最近の研究でSGLT2阻害薬のNa利尿は初期だけで、持続しないと言われています。おそらく腎でのNaを調整する機構が関わってSGLT2阻害薬によるNa利尿を調整しているのだと思います。ただし尿細管上皮細胞内のNa過剰は確実に起きていますので、SGLT2阻害薬による近位尿細管上皮細胞内でのNaポンプを回すためのATPの消費量軽減は、弱った腎臓を休ませてくれる可能性は大いにあると思っています。
Q.トリプルワーミーの論文間でリスク比がだいぶ違うのですが、その理由はどのようなことでしょうか?
A.トリプルワーミーの論文間で使っているNSAIDs、利尿薬、RAS阻害薬がみんなばらばらだからオッズ比に差があるのは当然です。NSAIDsだけでもセレコキシブのように腎機能に影響が少なく、心血管病変を起こしにくいものもありますが、ピロキシカムやメロキシカムのように半減期の長いオキシカム系は一般的に腎障害も胃障害も強いです。利尿薬だってサイアザイド系とループ利尿薬では利尿作用ははるかにループ利尿薬で強いですから、差が出て当然でしょう。また対象患者が日本人のように高齢者がほとんど、しかも後期高齢者が多いとなるとオッズ比は高くなりますから、対象患者の年齢や人種が異なることによって結果が異なることも考えられます。
SGLT2阻害薬のように併用によって急性腎障害が少なくなったという報告は前向きの大規模RCTのメタ解析によるものですから、リスク比・ハザード比がより均一なデータとして表れますが、トリプルワーミーの報告は薬剤師による後ろ向きの報告も多く、前向きの大規模RCTはほとんどないと思います。
Q.エンレストのバルサルタンの作用と抗利尿効果にNSAIDsを併用することはTriple Whammyとなるとお考えでしょうか。
A.エンレストもRAS阻害作用を持つので狭義のRAS阻害薬と考えていいと思います。それにNa利尿ペプチドの作用増強が加わりますので、降圧作用・利尿作用はRAS阻害薬より強く、カリウム上昇はRAS阻害薬よりも弱いです。となると脱水・降圧による腎機能悪化には気を付けるべきなので、Triple Whammyのリスクがあると今のところは考えています。ただしARNIはGFRを上げて腎保護作用を示すことからSGLT2阻害薬のようにAKIを予防する効果が出てくるかもしれませんが・・・・・。
Q.循環器疾患においてPCI後など低用量アスピリンを使用することが多く、RAS阻害薬が推奨されたりARNIが使用されるようになっております。その場合、心不全患者では既にダブルワーミーとなる場合が多くあると思います。やはりそういった患者様も腎障害リスクは高くなるのでしょうか?
A.心筋梗塞後で梗塞部位の大きければ心不全は必発です。心不全ではRAS阻害薬またはARNIの投与が必須になります。PCI後は低用量アスピリンを含めた2剤の抗血小板薬の併用は12か月は必要です。低用量アスピリンが腎機能を悪化させるかどうかは不明ですが、心不全の自覚症状が強くなれば利尿薬が必要になりますので、これらの薬物療法のそれぞれが腎障害リスクを上げる可能性があります。また心腎連関によって心不全自体が腎機能を悪化させます。
第18回 基礎から学ぶ薬剤師塾 Q&A
第 18回 基礎から学ぶ薬剤師塾 Q&A
広げてみようTDMの世界
~薬剤師が主役になれる薬物療法~
講演中にいただいた質問
沼津市立病院 平野雄一先生
Q1.腎機能が分からないときにシスタチン Cの依頼をしますが、返ってくるのが遅いです。その間のバンコマイシンの投与はどうすればよいのでしょうか?
A.おそらく腎機能低下患者にバンコマイシンを投与して数回目のトラフ値を測定していると思いますが、「測定したトラフ値が高いということは投与量が多すぎた=腎機能を高く見積もりすぎた」ということを表します。どの程度高かったかによって腎機能の見積もりの甘さを推測できます。バンコマイシンは尿中排泄率90%の薬ですので、腎機能の不明なときに投与するのは怖いことですが、逆にバンコマイシンの血中濃度測定によって、ある程度の腎機能をつかむことができます。多くの場合、高齢で栄養状態不良で活動度の低い患者さんがMRSA感染症に罹患しやすいのですが、このような症例では筋肉量が少ないために血清Cr値が低いので推算腎機能が高く見積もられるために用量過多になることが多いと思います。24時間畜尿による実測CCr(×0.715でGFRとして利用可能)またはシスタチンCによるeGFRの絶対値が分かれば、その後は血清Cr値が上昇しつつあるのか、低下しつつあるのかによって腎機能を追うことができます。
Q2.当院でのTDMの実施はバンコマイシンだけで終わっているが、次にやるとすれば何がおすすめですか?
A.バンコマイシンのTDMをやっているのであれば、抗菌薬のTDMを極めることから始めてはいかがでしょうか。テイコプラニン、アルベカシン、アミノグリコシド系抗菌薬、それに加えてボリコナゾールのTDMも開始すれば、院内でICTやAMT(抗菌薬適正使用推進チーム)で活躍できると思います。
ちなみに私の場合、1994年に100床以下の病院でも病棟での服薬指導業務を開始できるようになってから、通常のTDM対象薬の抗菌薬、ジゴキシン、テオフィリン、抗不整脈薬、抗てんかん薬、シクロスポリンに加えてアセタゾラミド、アシクロビルなどのTDM対象薬以外もHPLCを用いて測定することで、数か月で20種類近くのTDMを一挙に開始しました。薬剤科の人数は4~5人なのでHPLCを使用する薬物は担当性、つまりアシクロビルの依頼が来れば私が、ジソピラミドなどの抗不整脈薬の依頼が来ればAさんが研究室で前処理をして、検体をHPLCのある薬剤科に持って帰って分析していました。薬物動態的な解析(透析患者がほとんどなので解析ソフトはありません)をしたうえでのコメント記載は病棟でその患者さんの服薬指導担当者が記入することとし、最終的には私が内容をチェックしてからA4サイズの測定コメント付きの結果をカルテに貼付していました。つまり全員でTDMを担当していました。
TDMを開始する以前は仕事が終わってから午後6時くらいになって、ようやく研究(透析患者の中分子尿毒素、カテコラミン濃度の経時的変化、セレンなどの微量元素に関する研究)を開始できましたが、それはとても辛かったのです。でも透析患者のTDM自体が珍しかったこともあり、「原著論文が通常業務の一環として書ける」ということはとてもおいしいことだと思いました。
講演中にいただいたチャットでの質問
たかだ調剤薬局 永石潤先生
Q.TDM対象の薬剤の副作用の確認は行っていますが、先生はその他に薬局薬剤師に望むことはありますか?
A.クリニックの門前でも薬物濃度を測定することがあるはずです。ワルファリンだってINRを測定して、相互作用などによって異常値になることがよくあると思います(INRによるワルファリンの投与設計も広義のTDMといえます)。ジゴキシン、テオフィリンが当たり前に投与されていた1990年代には薬局薬剤師がTDMの解析をしていますという学会発表もありました。
例えば糸球体腎炎でシクロスポリンやタクロリムスの投与をしたり、抗てんかん薬を投与して血中濃度を測定することはクリニックでもあることだと思います。でもシクロスポリン濃度がいつもは100~200ng/mLだったのが800ng/mLになっていたらドクターは怖くなって投与中止してしまうかもしれません。実は単にトラフ値ではなく飲んだ直後のα相の採血だったというようなシンプルな間違いだと思いますが、薬物動態や相互作用に強くないドクターではやりがちなことです。だからクリニックでのTDMの解析やワルファリンの適正使用のお手伝いを申し出てはいかがでしょうか?
抗てんかん薬などもいのですが、くれぐれも濃度が低いだけで患者さんの病態を見ずに増量を申し出ないでください。抗てんかん薬の有効治療域には個人差がありますし、前回の薬剤師塾「薬物動態」で説明したように蛋白結合率低下によって、総クリアランスが低下するため、総濃度は低下しますが遊離型濃度は不変なことが多いので薬効は変化しないのです。患者さんを十分見ないで「血中濃度を直す」ことをTDMとは言いません。Therapeutic drug assayに過ぎません。Therapeutic drug monitoringによって患者さんの病態を観察して「患者さんを治す」ためにやっているのが本来のTDMですから。
国保多古中央病院 木内陽子先生
Q.全く基本的な質問ですが、トラフ採血を次回投与前の時間で代用してはいけないでしょうか。
A.トラフ値は、通常、次回投与直前の採血が望ましいとされています。一番低い濃度、つまりトラフ(谷底の意味)値ですから。
飯塚病院 田先由佳先生
Q.ガイドラインの改訂でCKDでのテイコプラニンの使用が増えそうな気がしました。あまり使用経験がないものの安全なイメージなのですが、副作用などのモニタリングのポイントはありますか?
A.僕もテイコプラニンのどの副作用をマークすべきなのかよくわからないくらい安全なイメージを持っています。だから副作用として聴覚障害や肝障害や腎障害など言われていますし国家試験にも出題されていますが、これらの経験をされた医師・薬剤師は非常に少ないと思います。蛋白結合率90%ですが、低アルブミン血症や尿毒症では蛋白結合率が低下し、遊離型のクリアランスが増大して総濃度は低下します。このことについての詳細はテイコプラニンが6種類の混合物であるため不明ですが、これによる増量によって起こった有害反応の例をあまり聞かないので、やはり安全性の高い薬物と考えてよさそうです。
ポイントは半減期が長いので初回負荷投与を躊躇しないことだと思います。新しいガイドライン2022でも腎機能に関わらず初日10~12mg/kgを2回、2日目10~12mg/kgを2回、3日目10~12mg/kgを1回で初回負荷投与をやっているって、初日からなんで1回2000mg程度の負荷投与をしないんだろうと思っています(平田の個人的な感想です)。初日の1回10~12mg/kgでは初日から有効濃度になるとは思えません。感染症は急性疾患ですから初日から効果を示さず、2~3日目から有効濃度になるようなやり方は、いい加減のやめてもらいたいと思います(これも平田の個人的な感想です)。
それからバンコマイシンによる腎障害が心配な症例、心内膜炎,骨関節感染症などの炎複雑性感染症では,目標トラフ値20~40 µg/mL(通常は15~30)を考慮します。バンコマイシン、テイコプラニン無効な症例ではリネゾリドやダプトマイシンなどをうまく使い分けてください。
講演後のアンケートでいただいた質問
熊本赤十字病院薬剤部 古庄 弘和先生
Q.90歳35㎏のサルコペニア高齢者にVCMを投与した症例において、シスタチンCの測定を考慮するとありましたが、私自身はどのような状況であれ、あまりシスタチンCの測定自体を医師に提案したことがありません。シスタチンCは保険診療請求で3月に1回しか測定できなかったり、外注で制約が多かったりするためです。腎機能が悪くなってしまった状態や、AKI発生により腎機能が変動している段階での測定では意義も低いように感じます。
サルコペニア高齢者であってもVCM開始のタイミングで測定を提案するには抵抗があり、シスタチンCはどういった患者にどのタイミングで測定を提案するべきでしょうか?
A.サルコペニア患者では血清Cr値による腎機能の絶対値は全く役に立ちません。だから実測CCrの測定か、それが無理ならシスタチンCの測定を、私は推奨しています。でも実際には沼津市立病院の平野先生への Q1 の回答と同じく、「測定したトラフ値が高いということは投与量が多すぎた=腎機能を高く見積もりすぎた」ということを表します。どの程度高かったかによって腎機能の見積もることができますので、これで十分対応できるように思います。
何もないときにシスタチンCの測定依頼をすることはあり得ないので、どのタイミングかといえば、VCM投与開始時になると思います。AKI発症により腎機能が変動している段階での測定ではシスタチンCの測定意義が低いのはおっしゃる通りです。古庄先生が医師にシスタチンC測定依頼を躊躇されるのはなぜ?僕はおそらく「シスタチンCってなに?」という医師がほとんどだからじゃないかと思います。腎臓内科医はもちろん測定経験がありますが、泌尿器科の先生はシスタチンCをもちろん知っていますが、測った経験者は非常にまれで、他科の先生はほとんどが「シスタチンCってなに?」という先生がほとんどだと思いますから。それでも何例かでも測定していただくことができれば、シスタチンCによるeGFRと血清Cr値によるeGFRあるいは推算CCr×0.789によるeGFRの乖離を体感できると思います(でもこのような場合、一番信頼できる腎機能マーカーは実測CCrだと思っています)。
バンコマイシンを投与する対象は多くの場合、高齢で栄養状態不良で活動度の低い患者さんがMRSA感染症に罹患しやすいので、このようなときに薬剤師がもっと医師にシスタチンCの測定を当たり前に依頼するようになれば、3か月に1回のみという制限も撤廃され、検査費用も1回1000円以上という価格も安くなるのではと思うのは私だけでしょうか。
松戸市立総合医療センター 井上大樹先生
Q.いつも大変貴重なご講演ありがとうございます。講演の中で、バンコマイシンやアミノグリコシドのピーク値採血のタイミングのお話がありましたが、病態や腎機能障害の有無、投与方法などにより分布相の延長や短縮などが発現する場合はございますでしょうか。ご教授いただけますと幸いです。
A.アミノグリコシド系抗菌薬の分布は細胞外液のみですので、末梢の毛細血管から間質液の移行にはほとんど個人差はないように思います。浮腫があると分布容積は増大しますが、ほぼ瞬時平衡に近いと思いますので分布相の時間の個人差はほとんどないでしょう。
バンコマイシンでは静注投与後の分布は各臓器によってさまざま濃度が異なりますから、病態や体格の個人差はありえると思いますが、具体的にそれらについて論じた報告はないと思います。「vancomycin×prolonged distribution time」で一応PubMed検索してみましたら何と21論文がヒットしましたが、決定的な論文は見つかりませんでした。
ただしUpToDateではバンコマイシンの分布容積に関しては「Adults: 0.4 to 1 L/kg (ASHP/IDSA/SIDP [Rybak 2009]); 0.3 to 0.5 L/kg in patients who are morbidly obese (Adane 2015; Bauer 1998; Hong 2015).」と記載されており、肥満患者ではVdが非常に小さいそうです。同じくUpToDateによるとピーク値測定について以下の記載がありました。「点滴終了後1~2時間を分布後のピーク濃度(Cmax)としているものの、定常状態に近い投与間隔での分布後ピーク濃度が望ましい」という記載は前半部分(赤字)と後半部分の内容(緑字)が著しく矛盾していますね。
UpToDateのTiming of serum samplesでの記載
投与1~2時間後に測定した分布後ピーク濃度(Cmax)と投与間隔の終了時に測定したトラフ濃度(Cmin)の2つの血清濃度の収集が必要である。定常状態に近い投与間隔での分布後ピーク濃度及びトラフ濃度を用いることが望ましい(可能であれば)。ベイズ法による AUC モニタリングでは、定常状態の血清濃度を必要としない(ASHP/IDSA/PIDS/SIDP [Rybak 2020] )。
≪ 2022.10.08 ≫ I&H平田塾「基礎から学ぶ心房細動治療薬と症例」での質問
Q.どの不整脈薬がどのタイプの不整脈に効果的という考え方がよく分かりません。1b群の抗不整脈薬が上室性の頻脈に効かない理由について心房筋の活動電位持続時間は短い為、APDを短くする1b群は効かないと聞いた事がありますがこの理解で合っていますか?
A.Vaughan-Williams分類Ⅰb群の中でもアプリンジンは上室性不整脈に効きますが、リドカイン、メキシレチンは心室性不整脈のみにしか効きません。その理由はおっしゃる通り「心房と心室ではAPDが異なり心房で短いためリドカイン、メキシレチンが心房のNaチャネルと結合できる時間は限られているので、不活性化状態にある時間が短い心房筋では効きにくい」で合っています(私も詳しくないです。ごめんなさい)。
心筋梗塞後の心室性不整脈患者にⅠc群の抗不整脈薬を投与すると不整脈に起因する心停止やすべての心停止がプラセボ群に比し有意に高かったという1991年のCAST study以降、循環器医による抗不整脈薬の投与は少なくなりました。致死的な心室性不整脈(心室細動、心室性頻拍、低心機能または肥大型心筋症に伴う心房細動)にアミオダロンなどを使わざるを得ないようなケースなど、極めて危険な不整脈にまれに処方することはありますが、危険な不整脈に関しては薬物療法以外のデバイスが進歩していますので、近年、循環器医が抗不整脈薬を投与することは多くはありません。ということで私自身は「薬剤師が不整脈という幅広い病態をすべて理解する必要はないけど、心房細動は心原性脳塞栓、心不全への移行が非常に怖いのでよく理解しておこう。あとはQT延長を起こす抗不整脈薬(ベプリジル、Ⅰa群、Ⅲ群のすべて)、WPW症候群による心房細動でレートコントロール薬の投与は心室細動に移行するため投与してはいけないなど、薬剤師が知っておくべきポイントをつかんでおけばいい」と大学での薬物治療学の講義で教えてきました。
平田への講演依頼に関しましては平田のメールアドレス
hirata@kumamoto-u.ac.jp までお気軽にご連絡ください。
第17回 基礎から学ぶ薬剤師塾 Q&A
第 17回 基礎から学ぶ薬剤師塾 Q&A
物性から薬物動態を理解してみよう
~「動態=薬の顔・特徴」だと思えば難しくない(2)~
チャットでの質問について
質問を4ついただきましたが、その内容をコピペし忘れておりました。そのため、一部、どの先生からの質問かが不明になってしまいました。申し訳ありません。
①チャットによる質問
高田調剤薬局 永石 潤先生
Q.デエビゴⓇ(レンボレキサント)は半減期が長いのですが、頓服でも有効でしょうか?
A.断っておきますが、私は、向精神薬の薬理についてはあまり詳しくありません。「レンボレキサントは、2種のオレキシン受容体サブタイプ(OX1R及びOX2R)の両者に対し、競合的かつ可逆的拮抗作用 を有するオレキシン受容体拮抗剤である。OX1R及びOX2Rの両者に親和性を示し、結合及び解離を示した(in vitro)。」とインタビューフォームにあり、これだけでは、血中濃度依存的に効果を示すかどうかは分からないのですが、血中濃度依存的と仮定してお答えさせていただきます。
初回投与時から効きますので、頓服でも効くはずです。でないと不眠症治療薬として臨床使用できるはずがないと常識的に考えます(インタビューフォームには「不眠症患者に対するレンボレキサント投与により、客観的評価による夜間後半部分の中途覚醒時間の短縮が認められた」とあります)。レンボレキサント10mg単回投与時の消失半減期は56.15時間と長いのですが、10mg投与後のCmaxが2時間で約36ng/mLですが、投与5時間足らずには約15ng/mL未満に低下しており、半減期は約3時間未満になります(図:インタビューフォームより)。ただしその後、血中濃度は非常に緩やかに消失し、24時間後もゼロにはなっていません。ですからレンボレキサントは1-コンパートメントモデルに適応する薬物ではなく、マルチコンマートメントモデルに適応するのだと思います。消失半減期は長いのですが、分布が終了する前のα相の濃度が高くなるため、催眠作用を示すのではないでしょうか。あくまで私の予想ですが・・・・。
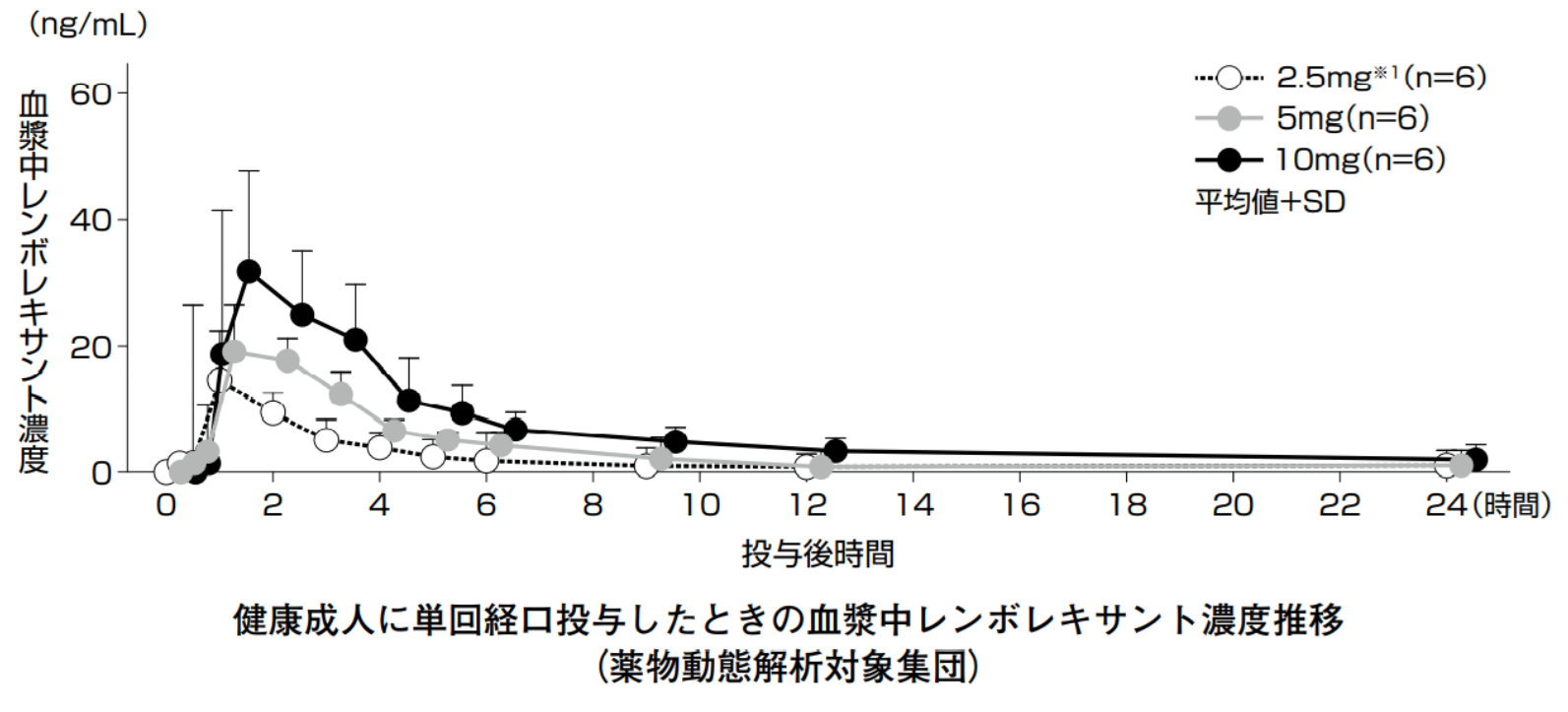
ベンゾジアゼピン系のニトラゼパムやジアゼパムも半減期はそれぞれ、26時間、20~70時間ととても長いですが、早朝覚醒しにくいような薬ではありません。
この図のように採血を何度も行うと、薬物によっては2コンパートメント、3コンパートメント以上の薬物があり、消失相もβ相だけではなく、γ相やδ相が認められることがあります。例えばアミノグリコシド系抗菌薬のゲンタマイシンは、薬物によって抗菌力や抗菌スペクトルは異なるものの、薬物動態は同一のパラメータを使えます。例えば腎機能が正常であれば半減期は1~4時間ですが、採血ポイントを増やすと血液から間質液に移行するα相(半減期は極めて短い)が認められますし、いわゆる臨床での消失相のβ相(1~4時間)が認められ、長期投与すると腎臓の近位尿細管上皮細胞に蓄積して、中止後、しばらくしても、腎臓に蓄積した薬物がじわじわと排泄されるため、半減期100時間のγ相が認められることがあります。この観察だけでもアミノグリコシド系を長期投与することが薬剤性腎障害のリスクであることが理解できますね。
あくまで個人的な予想ですが、分配係数log P=3.7と極めて使用性の高い薬物であるため、中枢か脂肪組織などに蓄積したレンボレキサントが、じわじわと溶出して肝代謝されているのかもしれません。
②アンケートによる質問
高田調剤薬局 永石 潤先生
Q.デエビゴⓇは反復投与でのCmaxが単回投与に比べて高くなりますが、頓用でも有効と考えて良いでしょうか?それとも連用すべきなのでしょうか?
A.私は薬理学の専門家ではないし、向精神薬についてはあまりよく知りませんので推測に過ぎないのですが、頓服で無効、連用しないと効かないような薬物は臨床で睡眠導入薬としては使い物になりませんから、レンボレキサントは頓服でも有効だと思いますし、連用しなくても効く薬だと思っています。でないと不眠治療薬としては使い物にはなりませんから。
確かにインタビューフォームを見ると10mgを14日間反復経口投与後のピーク濃度は70.2ng/mL で初回投与時のピーク濃度46.5ng/mLの2倍足らずになっています。これによってずっと眠ってしまうような薬物であれば、不眠治療薬としては不適格で、鎮静剤としてしか利用できないはずです。だからこの薬の薬理作用は血中濃度と相関しにくいメカニズムがあるのではないかと思っています。
たとえば抗血小板薬のアスピリンは不可逆的にシクロオキシゲナーゼを、PPIも不可逆的にプロトンポンプを阻害するため、血中濃度がゼロになっても薬効が持続するような薬物がありますし、抗うつ薬のように薬物の血中濃度とは無関係に2~3週間経過してから効果を表し始める薬物もあります。このように、薬物によっては必ずしも血中濃度と薬効がパラレルな関係にならないものもあります。
これらの回答はあくまで個人的な意見ですが、インタビューフォームの「治療の関する項目」「薬効薬理に関する項目」を見ると様々な臨床効果について記載されており、Cmaxが高くなることによる不利益はあまりないように思います。
③チャットによる質問
Q.定常状態になるまで薬物の効果が発現しないのでしょうか?
A.血中濃度依存的に薬効を示す薬であれば、半減期ごとの投与間隔で投与するとすれば、1回投与しただけで定常状態の50%になります。TDMの対象薬のように有効治療濃度域が狭い薬物でも、目標濃度の1/2で全く効かない薬は少ないと思いますので、多くの薬が1回目でも効果があると思います。ただし2回目の方が、よりよく効くでしょうし、3回目の方がもっと効くはずですが、定常状態になるとそれ以上投与しても効果は望めません。これは先述のように血中濃度依存的に薬効を示す薬の場合です。
頓服で効果を示す薬が多くあるように、定常状態にならなくても効果が発現するものも多くあります。またフロセミドのように半減期が0.3~1.5時間と短い薬は、初回投与時から定常状態になっていると考えてよいでしょう。
また前問②のようにたとえば抗血小板薬のアスピリンは不可逆的にシクロオキシゲナーゼを、PPIも不可逆的にプロトンポンプを阻害するため、服用後の時間がかなり経過して、血中濃度がゼロになっても薬効が持続するような薬物がありますし、抗うつ薬のように薬物の血中濃度とは無関係に2~3週間経過してから効果を表し始める薬物もあります。また講演でお話ししたようにアミノグリコシド系やキノロン系などでは血中濃度がゼロになっても殺菌効果が持続するpost antibiotic effect(PAE: 抗菌薬残存効果)が認められることがあります。
④チャットによる質問
Q.バンコマイシンの血中濃度が上がらない人がいます。どのような理由が考えられるのでしょうか?
A.ICUに入院している若年男性では、血管作動薬が投与されたり、全身熱傷で大量輸液などをすると、ARC (augmented renal clearance: 過大腎クリアランス)といって腎機能が高くなってバンコマイシンなど腎排泄性抗菌薬の血中濃度が上がらないため、効かないことがあります。これらの患者では実際にGFRが150~200mL/minと高くなるため、1.5~2倍以上投与しないと血中バンコマイシン濃度が十分上がりません(図1)。
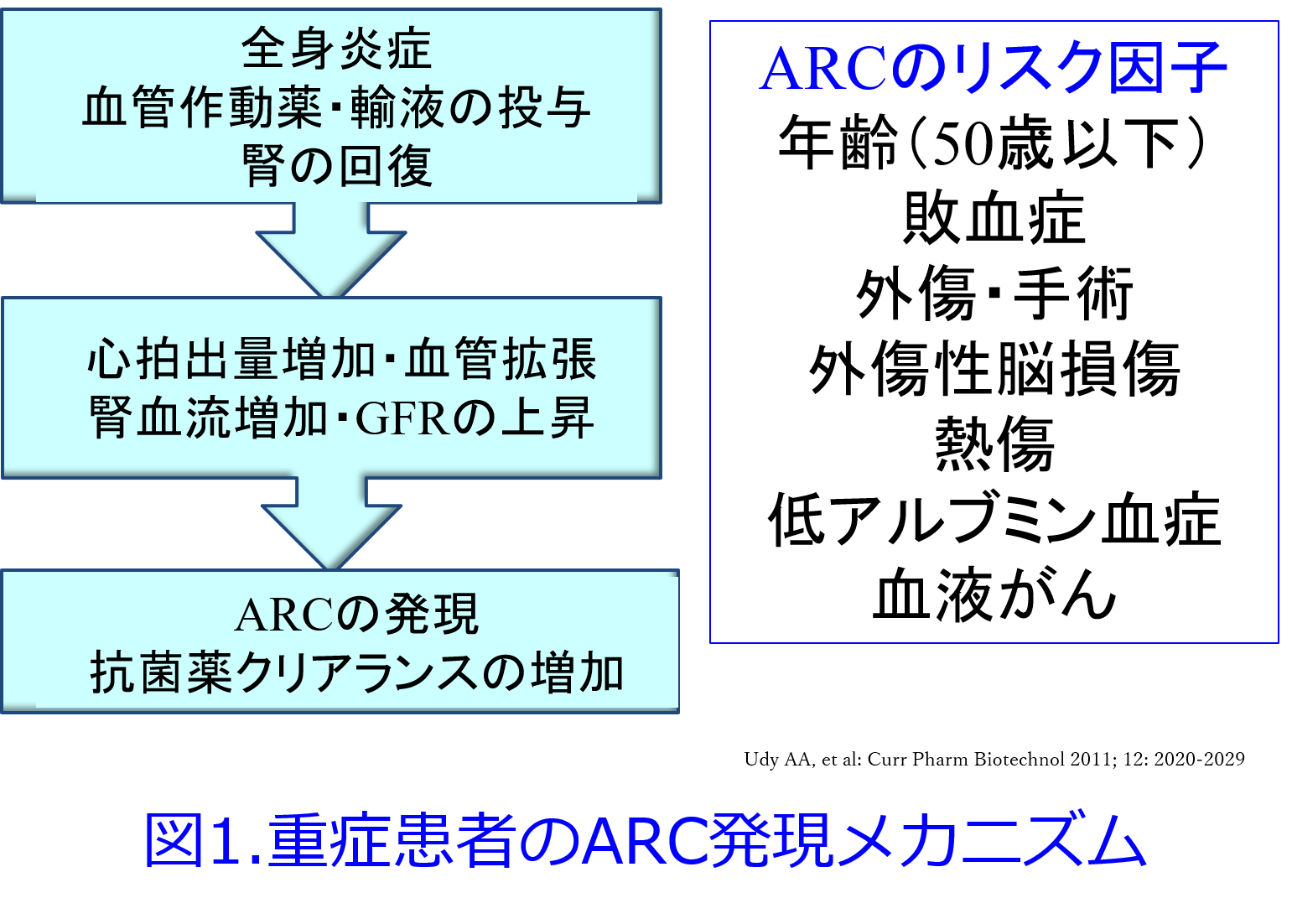
また糖尿病の初期の男性でもGFRが150mL/minになることはふつうに見られます。これは血糖値が非常に高いため、近位尿細管でSGLT2が過剰発現してブドウ糖とNaを一生懸命再吸収するため、尿細管腔中のNa濃度が低下し、それを感知したマクラデンサが輸入細動脈を拡張するという「尿細管糸球体フィードバック異常」になり、糸球体過剰濾過が起こるためです(図2)。そのためこの状態を放置しておくとアルブミンが尿中に漏出し腎機能が悪化するのが典型的な糖尿病性腎症です。それを防ぐためにRAS阻害薬やSGLT2阻害薬の投与が推奨されています。この状態でも腎機能が高いため尿中排泄率90%と総クリアランスの90%が腎クリアランスを占めるバンコマイシンの血中濃度は総クリアランスの増大によって上がりにくくなります。血中濃度=投与量/総CLですからね。
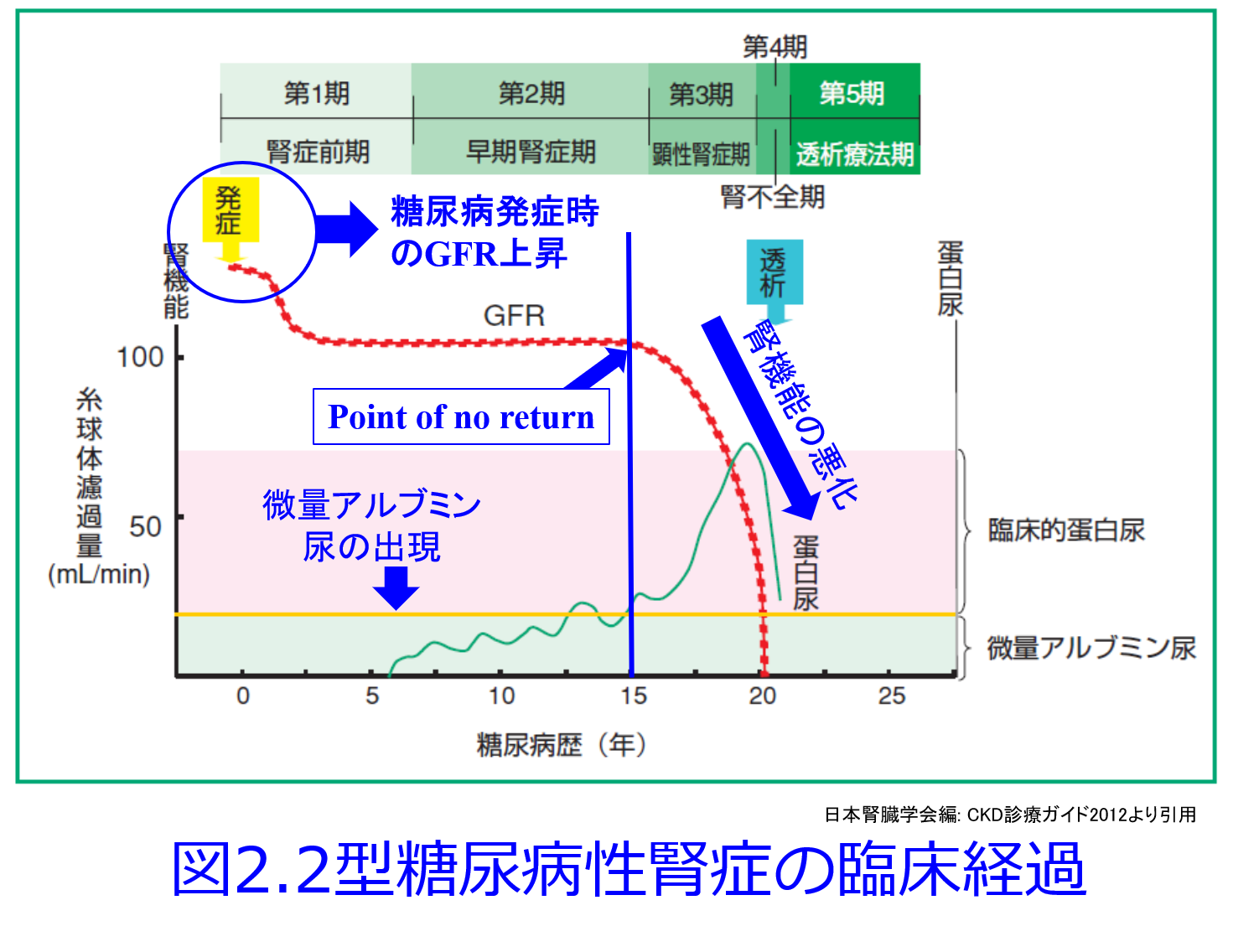
これらの方々は血清Cr値が男性なのに0.5mg/dL程度と低く、eGFRが150~200mL/min/1.73m2になることがありますが、これは痩せた高齢者のように腎機能が過大評価されたのではなく、実際に腎機能が高いのです。
⑤チャットによる質問
Q.妊娠中の体重増加時には推算CCrの式に標準体重を用いてよいのでしょうか?
A.妊娠時には血圧が上がり、腎血流も妊娠前に比し約30%上がり、GFRも妊娠前に比し50~60%程度上昇し、糸球体に負担がかかるため妊娠高血圧腎症になることがあります。そのため、血清Cr値はほぼ半減しますが、これは腎機能が過大評価されているためではなく、実際に腎機能が高くなっているためです。しかも妊娠第1期、2期、3期と腎機能が変化する可能性があります。ただし妊娠時に腎排泄性の薬物を投与することはまれでしょうが、感染症か何かでしょうか?「何のために腎機能を知る必要があるのか?」について、もう少し情報が欲しいところです。妊娠時の腎機能の推算について聞かれたのは私にとって初めての経験ですが、妊娠時の腎機能把握するための標準は24時間畜尿の実測CCrになります。
でもそれは簡易に測定できるものではありませんので、「pregnancy × estimation of renal function × body weight」でPubMed検索したところ、85論文がヒットしましたが、「CG式の計算式には妊娠前の体重を使用した。(140 – 年齢 × 体重 [kg] × 0.85)/72 x 血清Cr (mg/dL). CCrについては第1期26例、第2期33例、第3期21例、産後15例を比較し、蛋白排泄については第1期16例、第2期29例、第3期15例、産後15例を比較検討した。3つの期間を合わせたCCrの実測値(105±40mL/分[平均±SD])は、CGクリアランス(113±52mL/分;r = 0.87)と有意な相関があった。」1)と記載されていますので、妊娠前の体重を用いるのがよいかもしれません。r=0.87ということは臨床で確実性は必ずしも高くはないけれども参考にできると思います。
その他の論文2)では妊娠時の腎機能をCG式、MDRD式、CKD-EPI式を用いた腎機能と胎児の大きさを調べた報告では、おそらく何も特別な記載がないので、実測体重が使われていると思います。
また妊婦の血清シスタチンC値は、妊娠第1期には0.89±0.12mg/lと高値を示し、第2期には0.651±0.14mg/lと有意に減少し(第1期と比較してp = 0.0000)、第3期には0.82±0.191mg/lに再び上昇した。出産後は0.94 +/- 0.12 mg/lに上昇した。血清シスタチンCと血清Crの間に強い相関が認められた。女性ではGFRとシスタチンC値との間に強い負の相関が認められた(r = -0.546, p = 0.000)。GFRとシスタチンC値の間には直線的な関係が認められたという興味深い報告もありましたが、どの体重を用いたかは不明です3)。
妊婦の実測CCrと各予測法で算出された推算CCrの間には計的に有意な強い相関が認められ、徐脂肪体重を用いると有意に低くなるが、実測値により近いクリアランス推定値が得られたという報告もありました4)。
ただし、正確な腎機能を知りたい場合には、実測CCrを測定することをお勧めします。
引用文献
1)Quadi KH, et al: Assessment of renal function during pregnancy using a random urine protein to creatinine ratio and Cockcroft-Gault formula. Am J Kidney Dis 1994; 24: 416-420
2)Morken NH, et al: Maternal glomerular filtration rate in pregnancy and fetal size. PLoS One. 2014 Jul 8;9(7):e101897. doi: 10.1371/journal.pone.0101897. eCollection 2014.
3)Babay Z, et al: Serum cystatin C in pregnant women: reference values, reliable and superior diagnostic accuracy. Clin Exp Obstet Gynecol. 2005; 32: 175-179.
4)Sawyer WT, et al: A multicenter evaluation of variables affecting the predictability of creatinine clearance. Am J Clin Pathol. 1982; 78: 832-838.
⑥アンケートによる質問
手束病院 楠本倫子先生
Q.以前バンコマイシンの血中濃度について質問させて頂きました。今日も説明して頂いたのでとてもよく理解できました。臨床の現場では、日本化学療法学会のPATと言うソフトを使っています。ピーク値は点滴終了後2時間の値だとすれば、このソフトに入力する時もピーク値として入力した方が良いでしょうか?点滴終了後2時間後と言う選択肢もあるので、迷いますが。
A.ごめんなさい。PATというソフトを使ったことがありませんので、よくわかりません。僕は透析患者のバンコマイシンのTDMをやっていましたので、ソフトは使えなかったので、使った経験がありません。
透析患者では非透析時半減期200時間と非常に消失が遅いため、点滴終了後2時間の採血をピーク値としても大過ありませんが、腎機能がよければトラフ値と消失相に入った点滴終了2時間以降の2点の延長線と点滴終了時の交点をピーク値とすべきでしょう。
⑦アンケートによる質問
森之宮病院 力石慶子先生
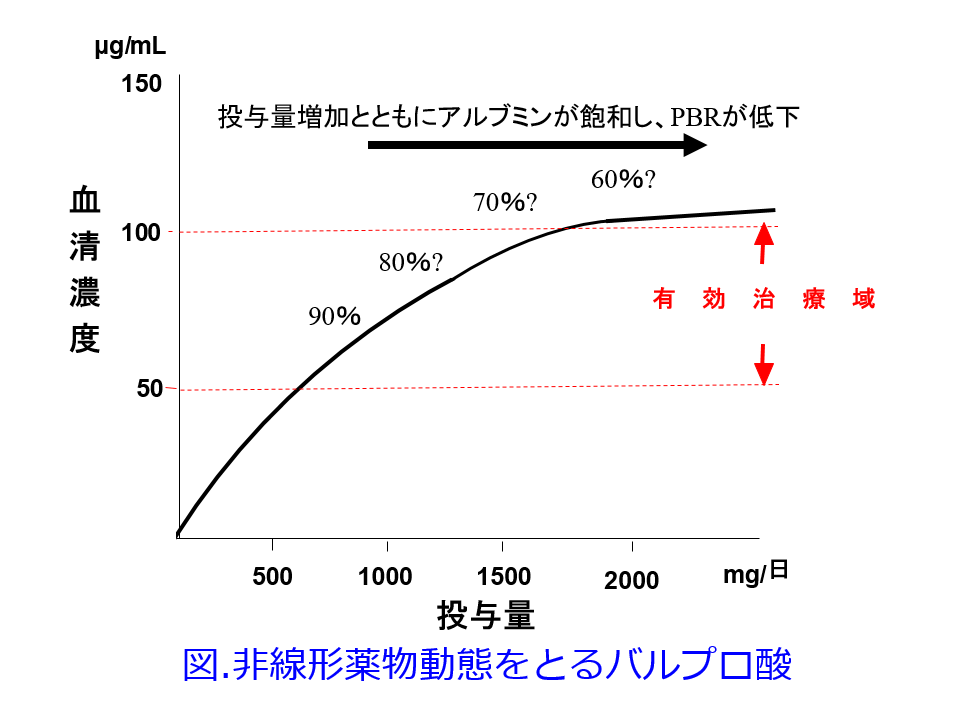
Q.低alb血症ではバルプロ酸の血中濃度が上がりにくいと思いますが、増量を続けていくうちに血中濃度が有効血中濃度まで上がってきました。この場合、血中濃度と効果をどう評価すべきでしょうか。組織へはかなり分布してしまうのでしょうか。血中濃度の割に傾眠はでやすいでしょうか。
A.バルプロ酸はフェニトインと逆の非線形薬物動態を示し、投与量が増えるほど、低アルブミン血症や尿毒症でも総血中濃度が上がりにくくなります。それで副作用がなく、てんかん発作が抑えられていればよいのですが、血中総濃度が低いからといって、増量すると遊離型濃度のみ上昇しますので、危険です(図)。総濃度のみを測定するTDMを実施することによって薬剤師が増量を提言して、副作用が起こってしまう最悪のパターンが想定されます。理想的にはアミコンフィルターを使ってフリー濃度を測定することをお勧めします。総濃度の有効治療域は50~100µg/mLで、腎機能正常者であれば蛋白結合率は90%と考えて、有効治療濃度が5~10µg/mLに入れるのが基本です。ただし抗てんかん薬は有効治療域以下でもコントロールできている人もあれば、有効治療域以上でも副作用を起こさずてんかん発作をコントロールできている人もいます。ですから、有効治療域にこだわるよりも発作が抑えられていて副作用が起こっていなければ、通常は投与量を変更しない方がよろしいかと思います。てんかんの専門医はそのようにしているはずです。
⑧アンケートによる質問
北見赤十字病院 加藤理愛先生
Q.知識不足でお恥ずかしいのですが、非腎クリアランスが上昇することでどんな問題が生じるのでしょうか?
A.ごめんなさい。お恥ずかしいのは私の方でした。最後のスライド「今回の研究のヒント」で、「末期腎不全患者では非腎クリアランスが上昇する」と書いており、言い間違いを連発していました。非腎クリアランスの「上昇」ではなく、「低下」です。訂正させていただきます(訂正版の図)。

2000年より以前では腎排泄性薬物では腎機能に応じて薬物投与量の減量をすればそれでよかったのです。そして、もちろん肝代謝型薬物は腎不全患者では減量をする必要はありませんでした。しかしFDAも日本の厚労省もメーカーに腎不全患者に投与したときの薬物動態を提示するよう求めたことから、様々な肝代謝薬物の血中濃度が末期腎不全患者で上昇することや腎排泄性薬物であってもGiusti-Hayton法で推測された腎機能別用量では血中濃度が上がってしまう薬物があることが明らかになってきました。
例えばサインバルタⓇのように尿中排泄率がゼロであっても高度腎障害患者に投与すると血中濃度が2倍になるため投与禁忌になっているような薬物が少なからずあります。この理由はおそらく尿毒素が蓄積したため、代謝酵素のCYP2C9や排泄トランスポータのP-糖タンパク質などの発現量やmRNAの発現量が低下して、薬物の代謝・排泄が低下するためと考えられています。ですから、高度腎障害、末期腎不全など、腎機能がかなり低下してから尿毒素が蓄積して血中濃度が上昇することが多いと思います。これらは非腎クリアランスの低下によって末期腎不全患者では血中濃度が上昇します。
平田への講演依頼に関しましては平田のメールアドレス hirata@kumamoto-u.ac.jp までお気軽にご連絡ください。
第16回 基礎から学ぶ薬剤師塾 Q&A
第 16回 基礎から学ぶ薬剤師塾 Q&A
物性から薬物動態を理解してみよう
~「動態=薬の顔・特徴」だと思えば難しくない~
チャットによる質問
①今井病院 粕谷美枝子先生
Q.薬物動態学が本当に苦手で大嫌いでしたが、平田先生のご講演を拝聴するたびに、その重要性を痛感しています。基本から勉強し直するためにお薦めの【薬物動態学】の参考書をお教え頂ければ幸いです。
A.僕も薬物動態学はむつかしい、特に難解な式を理解できないし、2-コンパートメントモデルなんて実臨床に本当に必要なの?と思っていました。薬物動態を身近にしてくれたのは現どんぐり工房の菅野彊先生が1998年に書かれた「わかる臨床薬物動態が理論の応用」という医薬ジャーナルの本でした。とても分かりやすい解説とかわいいイラストが薬物動態学のハードルを下げてくれました。僕にとっては革命的な本でした。ただし残念ながらこの医薬ジャーナル社は負債を抱えて事業停止になりましたので、この本は廃版になっていますが中古が手に入るかもしれません。
菅野彊先生はその後、「薬剤師のための『添付文書の読み方10の鉄則』改訂第3版( アドバンスクリエイト株式会社)」や「薬物動態を推理する55Question(南江堂)」を書かれていますし、どんぐり工房のお弟子さんの佐藤ユリ先生が「どんぐり未来塾の薬物動態マスター術 第2版(じほう)」を著されています。慶応義塾大学薬学部の大谷壽一先生の「マンガでわかる薬物動態学」を僕は読んだことがないのですが、大谷先生(九大大学院の時の僕のメンターです)の薬物動態学の講演はとても分かりやすく、濃い内容だったのできっと素晴らしい内容だと思います。これらの本をじっくり読んでいただけると薬物動態学を好きになるかもしれません。 それと僕の場合、このような入門書で、ある程度、薬物動態が理解できるようになったら、いわゆる大学で使っている教科書の加藤隆一先生の「臨床薬物動態学(改訂第5版): 臨床薬理学・薬物療法の基礎として」、緒方宏泰先生の「第4版 臨床薬物動態学: 薬物治療の適正化のために」「ウィンターの臨床薬物動態学の基礎―投与設計の考え方と臨床に役立つ実践法」などの教科書を3冊以上を読んで薬物動態理論を補強しました。よく売れているシリーズの「薬がみえる」vol.4は薬物動態学だけでなく薬力学や相互作用もかなり詳しく、そして分かりやすく解説されていますので、若い皆さんにはこれが一番かもしれません。
理解できないようなむつかしい数式を理解することはあきらめて、読み飛ばしていいのです。だって2-コンパートメントモデルなんて、何度も採血しないといけないので、臨床で使うのは無理があるし、分からないことはどうやっても分からないのだから!でも、これらの複数の教科書を読むと、すでに入門書で理解したことであっても、もっとわかりやすく理解できるようになるヒントが隠されていますし、「これって実臨床に使えそう」、「以前に体験した症例はこれで説明できる!」という薬剤師としての「気づき」が臨床薬剤師としての実力をアップしてくれるのだと思っています。

②たかだ調剤薬局 永石潤先生
Q.アセトアミノフェンのお話がありましたが、胃腸障害の副作用はないと考えてよろしいでしょうか?
A.僕が米国で研修させてもらった大学病院でもがん患者さんに「痛いときに」頓服でアセトアミノフェン650mg錠を6回分/日(3,900mg/日)、痛みのある多くの患者さんに投与されていました。癌性疼痛がきつくなれば服用錠数が徐々に増えるので、服用錠数が痛みのVASスケールの役割をして、0錠から2錠、4錠と増えることを強オピオイドの投与量を増やすマーカーにしていました。また米国の別の病院の小児科ではTPN(total parenteral nutrition)施行時、つまり絶食時の発熱や未熟児の発熱に対しアセトアミノフェンの懸濁液が汎用されていましたが、これは解熱に用いる低用量投与では胃障害が少ないことの裏づけと考えてもよいでしょう。
ただしアセトアミノフェンは用量増加に伴い胃腸障害を起こすことがありうるため、鎮痛用量では空腹時服用は推奨されません。日本ではアセトアミノフェンは添付文書上では解熱目的には1回300~500mg を頓用とし原則として1日2回まで、鎮痛目的には1回300~500mgを4~6時間おきとなっています。
NSAIDsを空腹時に飲むとのたうち回るような強烈な胃障害を起こしますが、OTC薬のタイレノールのパッケージには「空腹時にものめる優しさで、効く」と書いてあるように、NSAIDsに比べると胃障害は格段に弱いのですが、日本の添付文書では解熱用量でも添付文書上は空腹時の投与は避けることが望ましいとなっており、特に用量が多いときには胃障害を起こしやすくなるため、食後に投与すべきだと思っています。
③平成横浜病院 廣瀬里美子先生
Q.体重が多いのは一口に腎不全による浮腫であったり筋肉であったり脂肪太りだったりと色々ですが薬物動態の違いはどう理解すればよいでしょうか。基本的でお恥ずかしいのですがアドバイスお願いします。
A.薬物動態における「体重」の判断は薬用量の設定時にどう判断するか?という質問だと思って回答させていただきます。
筋肉が多い人は病気しにくいのですが、ジゴキシンはNaポンプ阻害薬なのでNa+-K+-ATPaseの豊富にある筋肉には血中濃度の10~20倍、心筋には30~50倍の濃度で分布するため、分布容積が大きくなります(初回負荷投与するとすれば多めに投与する必要があります)。でも患者さんの薬用量はジゴキシンが腎排泄性であるためVdではなく腎機能、つまり腎クリアランスによって決まります。
浮腫であれば間質液が増えていますので、細胞外液のみに分布する親水性薬物(脂質二重層を通って細胞内に移行できない薬物)の投与設計では重要です。アミノグリコシド系抗菌薬やβラクタム系抗菌薬がそのような親水性薬物です。ではアミノグリコシド系抗菌薬に関する例題を解いてみましょう。
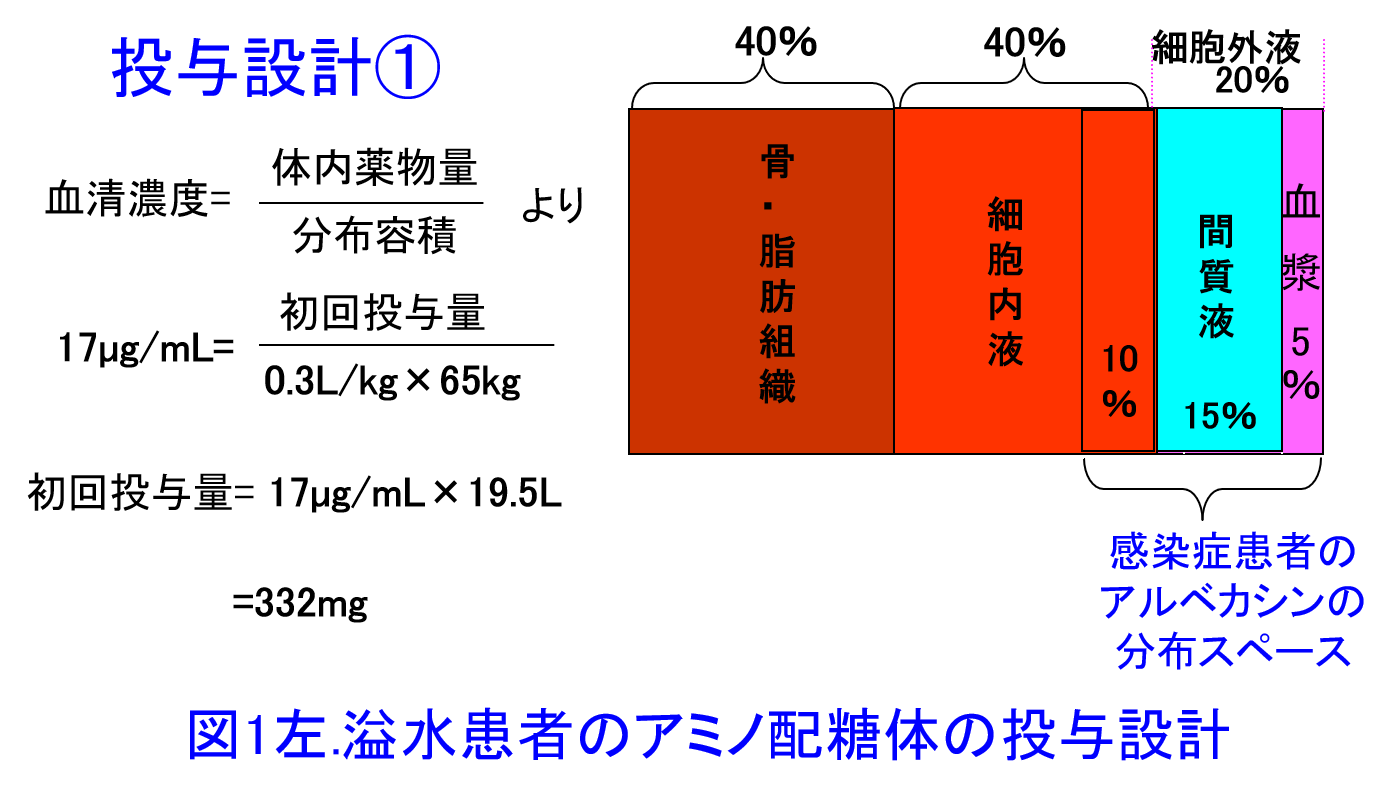
例題:通常時の体重が50kgの肝硬変患者がMRSA肺炎に罹患した。本症例は肝硬変による腹水を伴う溢水により体重が65kgに増加している。この患者にアルベカシン(ハベカシン®)の初回投与量の投与設計をどのようにすべきか。アルベカシンの目標ピーク濃度は17µg/mLとし、Vdは0.3L/kgとする。
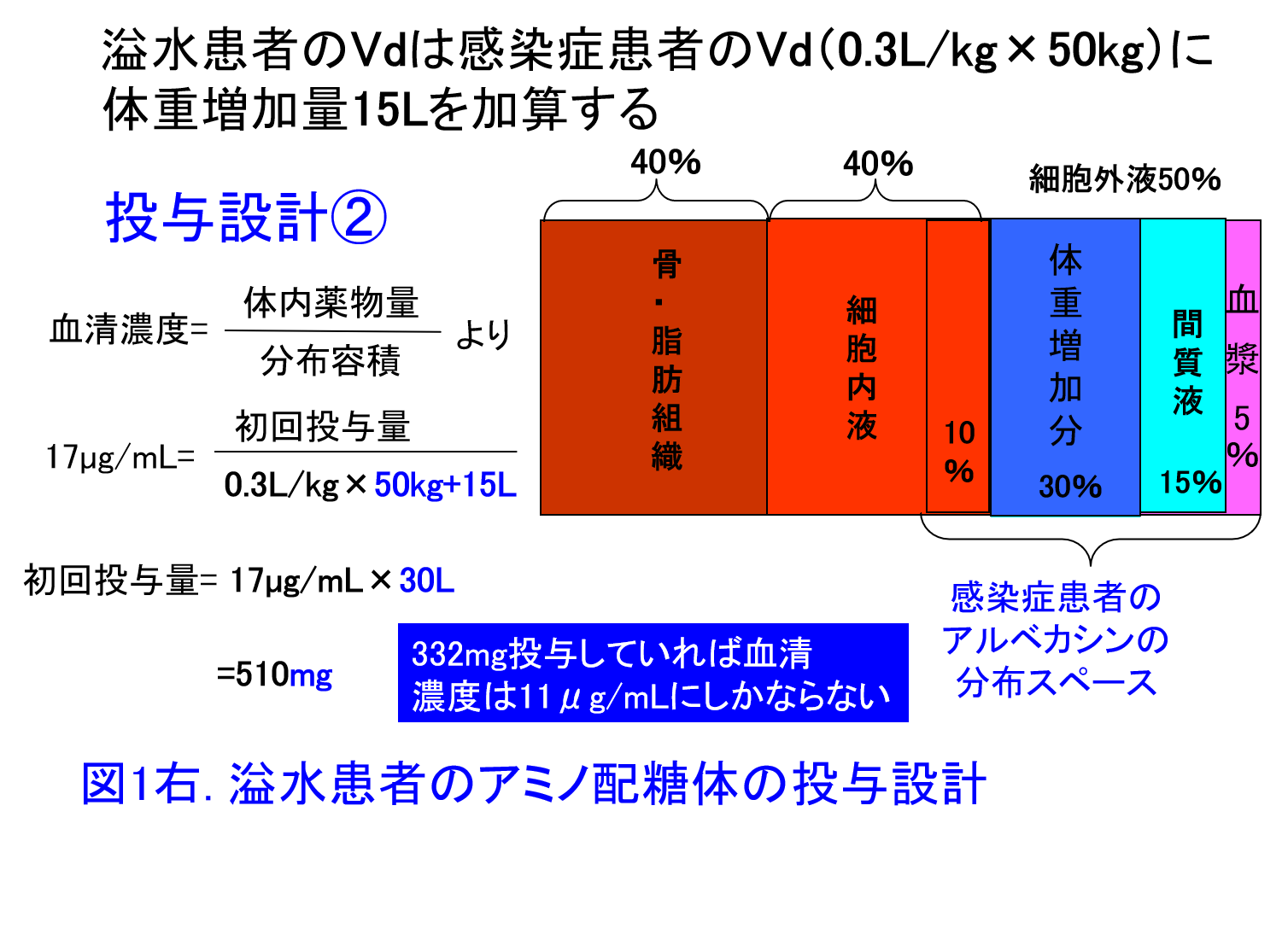
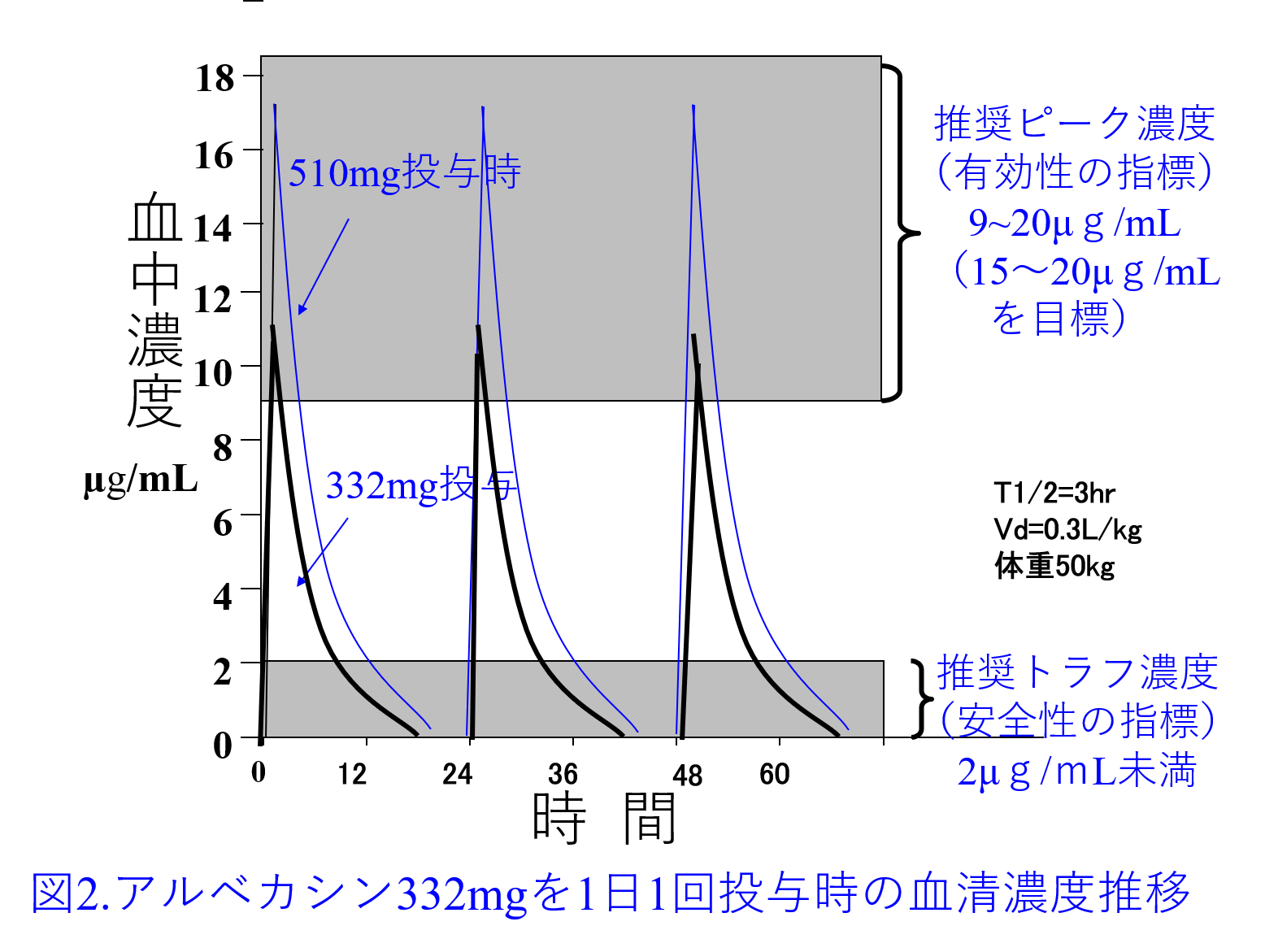
解答:アルベカシンXmgを65kgの患者に投与し17µg/mLを目標ピーク濃度にするとXmg/(0.3L/kg×65kg)=17µg/mLとなり、332mgを投与すると十分なピーク濃度を保てるはず(図1左)。ただし腹水は細胞外液のため、実際には通常体重50kgのVd 15L+腹水15Lが分布容積に近似すると考える。つまり溢水患者のVdは感染症患者のVd(0.3L/kg×50kg)に体重増加量15Lを加算して、Xmg/(0.3L/kg×50kg+15L)=17µg/mLとなり、目標ピーク濃度を17µg/mLにするならば510mgの投与量が必要(図1右、図2)。初回投与量は腎機能による差はありませんが、2日目以降は腎機能に応じた減量または投与間隔の延長が必要になります。
ただし本症例が肝硬変ではなく、末期腎不全による尿量減少によって体重が65kgに上昇しているとすれば、主治医には保存期腎不全患者であれば腎毒性のない他剤を選択すべきです。
添付文書には「1日1回150〜200mg(力価)を30分〜2時間かけて点滴静注する(2回に分けてもよい)」と書かれているので、医師の多くが「こんな大量投与したことがない」と言って引いてしまいますが、200mg/日では効きません。アミノグリコシドの添付文書のほとんどがピーク濃度が低いため効かず、ましてや2回に分けるとピーク値は下がりトラフ値が上がって、効きめはより弱くなって、腎障害が起こりやすくなります。
ただし浮腫があって体重が増えても腎機能がよくなるわけがないので(腎うっ血によってかえって悪くなることがあります)、eGFRや推算CCrに代入する体重は浮腫のないときの体重を使いましょう。
肥満患者で腎機能を推算するときに問題になるのが、推算CCrで身長が考慮されていないため、体重が2倍になると腎機能も2倍に評価されますが(図3)、脂肪太りの場合も、太ったために腎機能がよくなるわけではないので(一般的に肥満はCKDの進行要因になります)、太っていないときの体重は理想体重ですが、生来肥満気味の人は体重が多い分だけ、筋肉も使いますので、筋肉量も増えると考えると、通常、補正体重を使うのがよいとされています。
理想体重(男性)=50+{2.3×(身長−152.4)}/2.54
理想体重(女性)=45.5+{2.3×(身長−152.4)}/2.54
補正体重(kg)= 理想体重+[0.43×(実測体重-理想体重)]
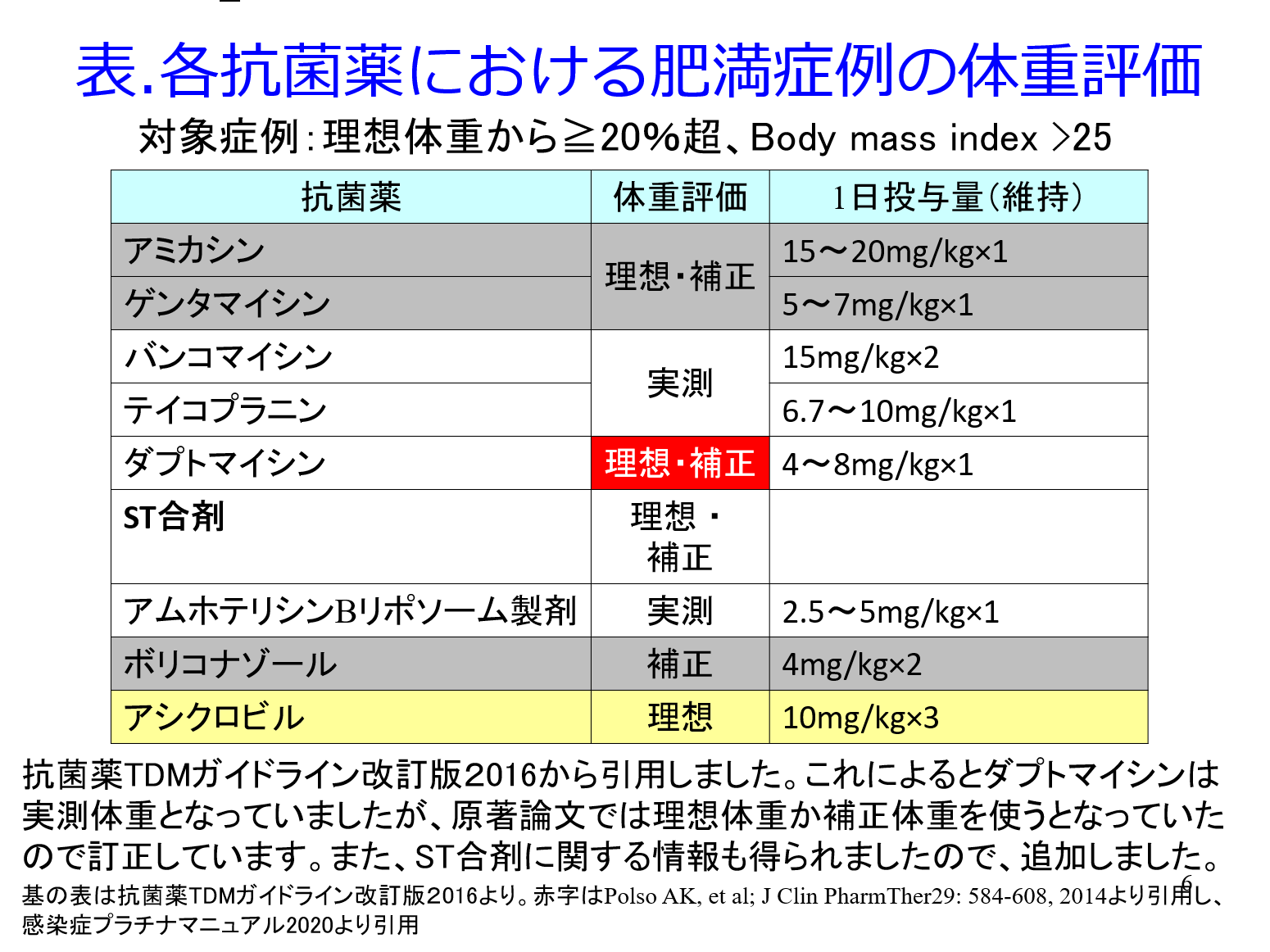
ただし薬物によって体重の評価に何を使うのかが異なります(表)。僕自身は組織に分布しやすい(Vdの大きい)薬物は実測体重、親水性の高い薬物は理想体重を使うイメージを持っています。例えばバンコマイシンは実測体重を用いますが、米国の病院で200kg以上の肥満患者がMRSA敗血症で入院してきて「スミオ、バンコマイシンのトラフが5µg/mLにしかならないのよ」と相談を受けましたが、投与量は4gを超えて投与したことがないので、4gを初日投与したとのこと。PubMedで調べるとバンコマイシンは実測体重で投与設計することが分かったので、「8g/日投与しなきゃ効かないよ」と答え、実際に倍量投与してトラフ値が10以上になりました。
④伊奈オリーブ薬局 米坂由可里先生
Q.フェノフィブラート を肝機能低下傾向の方が服用していました。その後肝機能は改善しましたが、腎機能が悪化しました。どのように理解すればよろしいでしょうか?
A.この限られた情報で判断することはなかなかできないのですが、フィブラート系の投与によって腎機能が悪化すると、ふつうは横紋筋融解症による腎機能悪化を疑います。骨格筋が壊死して融解し、筋肉内の成分が血中に溶けだして、ミオグロビンが尿細管に詰まって急性腎障害が起こります。クレアチンキナーゼ上昇とともに LDH, AST, ALT などが上昇し、血尿が観察されれば、横紋筋融解症と考えてよいでしょう。フェノフィブラートの活性代謝物のフェノフィブリン酸の尿中排泄率は73%と高いため、腎排泄性薬物ですが、肝機能低下傾向患者に発症した理由はこれだけの情報では不明です。もしかして横紋筋融解症によってAST, ALTが高くなったため、肝機能低下傾向と判断したのではないでしょうか?
⑤今井病院 粕谷美枝子先生
Q.グリメピリド1mgを腎機能CCr35mL/minくらいの80歳代の患者さまに使用しており、低血糖症状と思われる症状が時々出るのですが、減量提案をしても処方医にあまり取り上げていただけません。認知機能も低下しており本人の自覚症状も薄いため、本日の先生のお話を聴いて低血糖症状の遷延化が不安になりました。 このような場合、減量提案よりも処方変更を提案した方が良いでしょうか。
A.腎機能の低下した後期高齢者の低血糖、とても危ないですね。SU薬とナテグリニドは重篤な腎機能低下(CCr<30mL/min)には禁忌です。CCr35mL/minであれば安全域の広い薬であれば投与しても構わないのですが、SU薬の低血糖と抗凝固薬による出血は超ハイリスク薬にあたる副作用ですからCCr<30mL/minには禁忌となっていてもCCr<50mL/minでも投与しない方が無難な薬と言えます。講演でお話ししましたように表に示すSU薬とナテグリニドには活性代謝物があり、それらは親化合物よりも親水性が高いため特異的に腎機能低下患者で蓄積しやすいのです。だからCCr35mL/minだからという理由でSU薬の投与にこだわる医師であれば、活性代謝物のないグリミクロンⓇ錠がより低血糖リスクが少ないので、変更を提案してみてはいかがでしょうか?以下の3点で理論武装しましょう。

①腎機能低下患者は遷延性低血糖が起こりやすく、重症低血糖はインスリン拮抗ホルモンであるカテコラミンの分泌を介して重症高血圧、低カリウム血症、QT延長→トルサード・ポアン→心停止など、心血管病変の悪化原因になるとても危険。
②活性代謝物のあるアマリールⓇ錠はインスリン抵抗性を改善する作用のある第3世代SU薬と言われているが、活性代謝物のないグリミクロンⓇ錠の方が安全。ミチグリニドが禁忌じゃないのにナテグリニドだけが禁忌なのは発売後に透析患者が重症低血糖事故が起こったため。
③80歳代でCCr35mL/minという腎機能は不可逆的に(進行性に)腎機能が悪化するため、重篤な腎機能障害でSU薬が禁忌になる腎機能になるのは間近です。
時間内に回答できなかった質問
⑥南相馬市立総合病院 中島先生
Q.薬剤の効果の持続時間は薬剤が有効血中濃度域にある間と考えています。薬剤毎の有効血中濃度域はどのように調べたら良いのでしょうか
A.薬剤の有効治療域は常に有効下限以上の濃度でないといけないわけではありません。前述のようにアミノグリコシド系抗菌薬のように、トラフ値が低いほど腎障害が起こりにくいので、血中トラフ濃度がゼロになっても構いません。アミノグリコシド系抗菌薬やキノロン系のように殺菌力の強い抗菌薬にはPAE(post antibiotic effect:抗菌薬残存効果)があるため、MIC以下のゼロになっても抗菌メカニズムは持続しますから。このようにPKだけではなく、PDも考慮した投与設計が必要になります。
すべての薬に有効治療域が設定されているわけではありません。TDM対象薬であっても有効治療域が不明な抗てんかん薬があります。抗てんかん薬はアドヒアランス不良でてんかん発作を起こすため、アドヒアランスの確認の意味だけでもTDMを実施する価値があります。TDM対象薬の治療域に関してはこのブログ「育薬に活用できるデータベース」の「2.薬物動態・TDM」に知りうる限りの有効治療域が載っています。
⑦高砂市民病院 白木先生
Q.CYPの寄与率や阻害率を確認する方法はありますか。
⑦佐賀大学医学部附属病院 橘川奈生先生
Q.CYPの寄与率などを用いて計算できる薬剤についてご教示いただけますと幸いです。薬剤のプロファイルにより異なるかと存じますが、約何倍までですと安全性の面から許容されますでしょうか。
A.これらに関しましては僕は専門家ではないので、よくわかりません。鈴木洋史先生、大野能之先生の著された「これからの薬物相互作用マネジメント 臨床を変えるPISCSの基本と実践 第2版(じほう)」を参照してください。
例えばスタチン薬のシンバスタチンのFは5%と極めて低いのは、CYP3A4の寄与がほぼ100%のため小腸のCYP3Aによって初回通過効果を受けやすいから→CYP3A4を100%近く阻害するボリコナゾールやイトラコナゾールでは血中濃度が約20倍近くになるはず。そしてグレープフルーツを食べたりすると10倍近く血中濃度が上がるので、横紋筋融解症が起こりやすい→薬剤師はFの小さいシンバスタチン、アトルバスタチン、フェロジピンに関しては「グレープフルーツを食べたり飲んではいけません」という薬剤情報提供用紙を渡すだけではだめで、ちゃんと口頭でも注意しなくてはならない などの理論展開が可能になります。
薬の安全性は薬によって大きく異なります。βラクタム系抗菌薬は腎排泄性薬物でアレルギー性副作用が怖いが、安全性が高いので、初回負荷投与は思い切りいこう。だけど2回目以降も減量せず投与すると1週間くらいで数倍以上の血中濃度が持続すると痙攣をおこすことがあるので、腎機能低下患者や高齢者に減量せずに継続投与はあり得ない。抗凝固薬のダビガトランは超ハイリスク薬であるため、血中濃度はほんの数倍でも非常に危険です。繰り返しますが、薬の安全性はこのように薬によって大きく異なります。
フェニトインは非線形薬物動態を取るTDM対象薬ですから数10倍の血中濃度になると「致死濃度」になるかというと、30年前くらいに恐怖の「アレビアチン原末」が売られていました。僕はこれは危ないと思っていましたが、当時の精神科医は1包に複数の抗てんかん薬の散薬を混ぜて投与することを好んでいたので、カサの高い10倍酸はではなく原末を好んでいたため、製薬会社も危ない原末の製造中止に踏み切れなかったのです。そこで10倍散の代わりに原末を調剤したという薬剤師の誤薬が10件以上も起こったのですが、十数症例目の誤薬でようやく死亡例が出たのです。フェニトイン濃度は10倍ではなく、非線形であるため、数百倍あるいは1000倍近くになったのかもしれません。その時「非線形でTDM対象薬のフェニトインでも人はそう簡単には死亡しないんだ」と感じた方は多かったと思います。でもCCr<30mL/minで禁忌のダビガトランは発売半年間で24名が出血死しました。24名中22名が70歳以上の高齢者です。
これで何が言いたいかわかりますか?フェニトイン服用患者は結構若年者や青年患者が多いですよね。何倍という血中濃度だけではなく、70歳以上の後期高齢者は弱い!しかも心房細動は心不全をきたすことが多い。心不全でフレイル、サルコペニアの高齢者は極めて脆弱、という患者側の要因も考慮しなくてはならないということです。ちなみに皆さんの把握している薬物動態パラメータは治験時に行われた第1相試験、つまり「若年青年男子」が対象なのです。でも疾病の多くは高齢者に発症し、当然薬を飲む多くの人は高齢者ですよね。薬の専門家である皆さんは薬物動態パラメータのデータを高齢者に翻訳しなければならないのです!PBRはアルブミン濃度の低い高齢者では低くなるはず、tmaxは消化管運動の遅延する高齢者では遅延するはず、腎機能は当然低下するはず…………のようにです。
⑧道ノ尾病院 渕上朋一先生
Q.薬物動態について、理解がより深まる講演をありがとうございました。講演の中で、ファーマコジェネティクスと薬物動態の話しがでてきましたが、エピジェネティクス機構が薬物動態の個人差となることはあるのでしょうか?
A.僕はこの分野の専門家ではありませんが、双子であっても1人は喫煙者、1人は非喫煙者であればCYP1A2の誘導により、テオフィリンやプロプラノロールのクリアランスが2倍近くの差が出てくるはずですし、飲んでいる薬によって耐性、自己誘導などを起こしえますので、環境因子によって薬物動態は変わります。したがってエピジェネティクス機構が薬物動態の個人差となることは十分にあると思います。
第 15回 基礎から学ぶ薬剤師塾 Q&A
第 15回 基礎から学ぶ薬剤師塾 Q&A
透析を科学する
~CHDFでは透析よりも薬がよく抜けるのはなぜ?~
チャットによる質問
匿名
Q.エベレンゾⓇ(ロキサデュスタット)の透析性は?
A.蛋白結合率99%ですから全く透析で除去されません。
アンケートによるご質問
滋賀医大 福井先生
Q.CHDF時の用量設定について、透析機器設定から計算される腎機能と血液検査での腎機能に大きく乖離がある場合でも(無尿)、計算上で考えられる投与量を投与して問題ありませんでしょうか。
A.ごめんなさい。「透析機器設定から計算される腎機能」というのがよくわかりません。
薬局フォーリア 河村美弥子先生
Q.基本的なことで申し訳ないのですが透析クリアランスと透析性と同じ意味と思っていました。透析クリアランスは速度を表し、透析性というのは性質のことで、透析除去率というのは割合ということでしょうか???
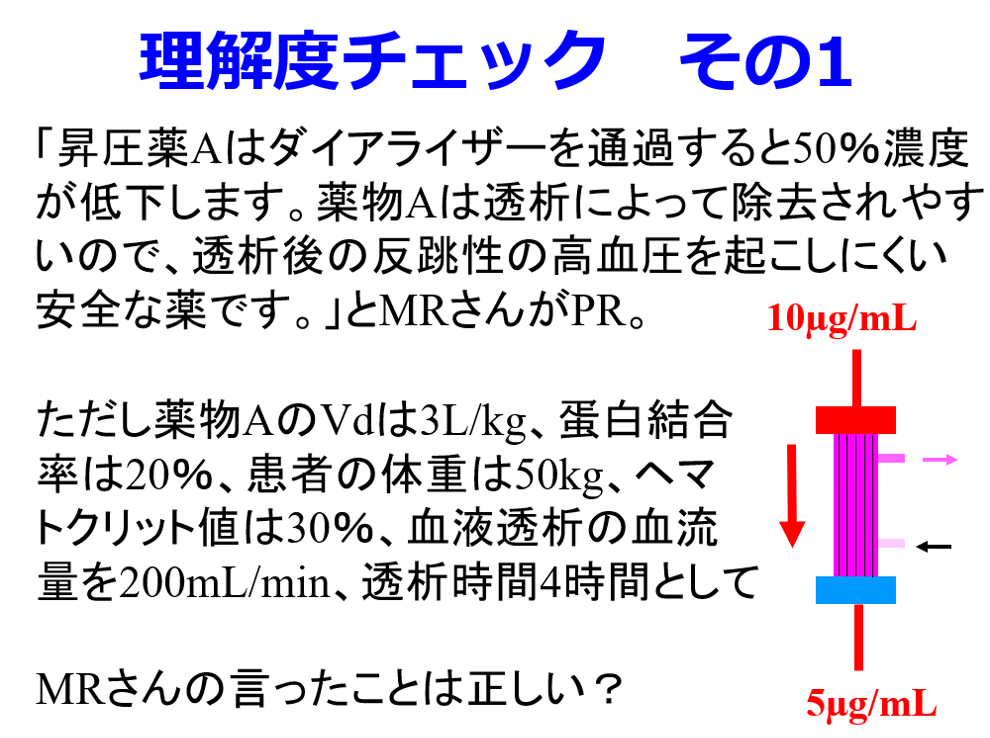
A.透析性は透析除去率と同じ意味で使われており、「薬物の透析による除去率(透析性)=1回の透析によって体外に除去された薬物量/もともと体内にあった薬物量」で通常は%で表されます(だから割合ですね)。透析クリアランスはクリアランスですから、単位時間あたりに浄化された液体の総量ですから通常はmL/minで表します(だから速度ですね)。いくらダイアライザークリアランスが高くてもVdが大きな薬物の除去率は高くなるとは限りません。講演の時に理解度チェックその1で昇圧薬のリズミックⓇの例を出しましたが、図に誤記があったために分かりにくかったと思いますので正しいものを示します。

佐賀大学医学部附属病院 薬剤部 橘川奈生先生
Q.HD・CHDF・PDでアンモニアの除去率に違いはございますでしょうか。また、リバウンドにも差がございますでしょうか。ご教示いただけますと幸いです。
A.分離量の小さいアンモニアは尿素と同様、血液浄化法でよく抜けます。ただし講演のスライドで示しましたように何らかの中毒症状の治療にCAPDは低クリアランスであるため有効ではないのと同様、日本のような低クリアランスのCHDFも有効性は低いと思います(これは平田の意見です)。ですから溶質の除去率はアンモニア以外も含めてHD>CHDF>CAPDになります。
それからHDのような急激な血液浄化法ほどリバウンド現象は強いのですが、持続的血液浄化法ではリバウンドはほとんど認められません。小児の高アンモニア血症のように250μmol/L以上の危険な状態で内科的治療が無効な場合には、間欠的HDが使われることがあります。ただし海外では高クリアランスのCRRTも実施可能なため、間欠的HDではリバウンドが危惧される場合には、持続的にアンモニアを除去するためにCRRTを高アンモニア血症の治療に用いられることもありますが、もちろんHDの方が除去性能は高いです。ただしその分、栄養素も短時間の間に急激に除去され体力を消耗するため、CRRTを選ぶこともあるようです。150μmol/L以下になれば治療を中止してよいそうです。ただし血液浄化時に除水をしてしまうと血圧が下がったり、腎虚血によって腎機能が悪化しますし、透析液は透析患者用のものなので、低リン血症、低カリウム血症にならないよう注意して血液透析を実施する必要があります。
これらの情報はおそらく大学病院では活用可能なUpToDateで「hyperammonemia×blood purification」を検索ワードとして情報を入手できます。
手束病院 楠本倫子先生
Q.バンコマイシンのTDMで採血ポイントはいつがベストでしょうか? 1回の時と2回採血する場合を教えて頂ければ幸いです。又、今まで安定していたトラフ値が突然倍近くになったり、腎機能が急激に悪くなるとすれば病態(敗血症のような重症例)によるものか、それとも腎機能が過大評価されていた可能性(CG式Ccrで判断)も否定できないのでしょうか?
A.患者さんはHD患者さんではなく、定常状態に達していると仮定して答えさせていただきます。1回の採血ではトラフ値、つまり次回投与直前の採血だけでよいでしょう。ただし重症感染症の場合、抗菌薬TDMガイドライン2022ではピーク濃度とトラフ濃度の2点採血を行ってAUC/MICを400-600としているため、2点採血が必要となります。バンコマイシンのピーク濃度は点滴終了後1~2時間となっておりますが、1時間は完全にα相(分布相)で、組織と血中濃度が平衡状態になっていません(図1)。2時間以降経過したβ相(消失相)で採血しないとAUCは過大評価されますし(図2:この図では大した差ではないように見えますが、腎機能が低下すればするほどAUCの過大評価が顕著になります)、ピーク濃度が高くなるということはVdが過小評価されます。私は透析患者のTDMをやってきたので、透析終了時から点滴を開始して、点滴終了後2時間(可能なら2時間以上経過した方が確実にβ相になるため望ましい)をピーク値として、次回透析前をトラフ値とし、その2点からKelの傾きを算出して点滴終了時の値をピーク値として採血することが多かったため、バンコマイシンのVdを0.9~1.0L/kgだと信じていますが、点滴終了後1時間で採血している病院ではVdが0.6L/kg程度を採用していると思います。透析患者さんでは非透析時のバンコマイシンの半減期は200時間程度と極めて消失が遅いため、点滴終了後2時間以降のの採血はあまり問題にはなりませんでした。
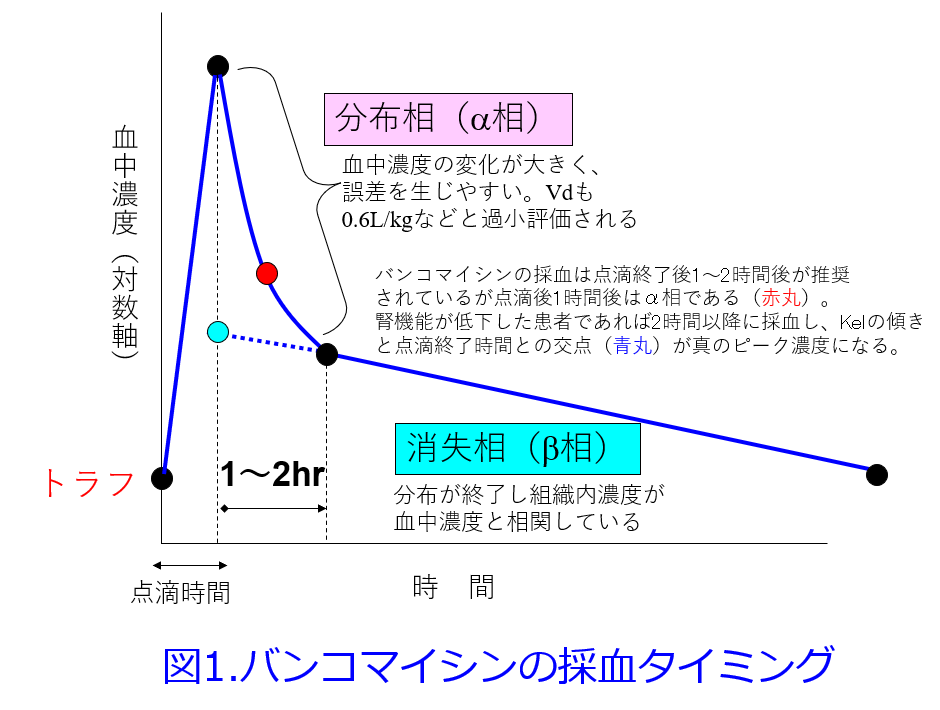
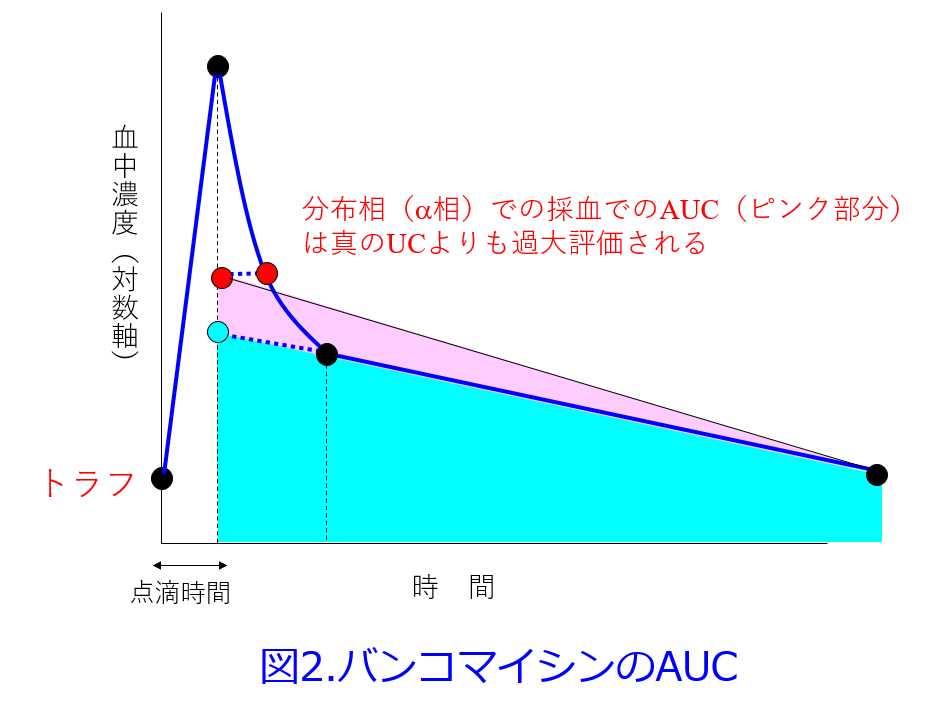
トラフ値が突然倍近くになったのはAKIの可能性があります。1つはバンコマイシンによるAKIも考えられますが、重症感染症のために脱水を来たしBUN/Crが30以上になっている場合には輸液をすることでBUNが急低下し、Cr値もやや下がることが多いですので、重症感染症での輸液管理は非常に大切です。それと重症感染症になりやすい方は痩せて栄養状態が不良の高齢者が多いですから、重症感染症が長引けば長引くほど、筋肉量が低下し、血清Cr値が低くなり、腎機能の過大評価をしてしまう原因にもなります。この際には24時間畜尿の実測CCr(×0.715でGFRとして評価できます)かシスタチンCによるeGFRの算出が望ましいと思います。 一般的には感染症に罹患しやすい高齢者ではeGFRの方が推算CCrに比べ過大評価しやすいです。だから感染症に携わっている薬剤師は推算CCrを使う方が多いです。
石川県小松市民病院 薬剤科 小川 依先生
Q.中規模程度の病院でICU担当薬剤師なのですが、CHDF、HD、CAPD患者さん、それぞれにおけるバンコマイシンの投与設計で迷うことがございます。
CHDFの患者さんに対しては山本武人先生のクリアランス理論に基づくCRRT患者の投与設計論文を参考にして、体重, QF, QDを元に投与設計をしています。残存腎機能を加えられることが臨床で役に立っておりこちらを使うことが多いのですが、今日の講演で先生がご提示して頂いた20mg/kg loadingから、7.5-10mg/kg維持で投与計画を行い、そのあとの血中濃度でフォローする方法も一考なのでしょうか。サブラットの適応もあり、QF+QDがそれほど変化することもないため、確かに特殊な条件とならなければ、固定量投与も一考かと愚考いたします。
そしてもう一つ悩ましいのがCAPD患者さんのバンコマイシン投与設定です。HD患者さんはある程度明示されたものがあるのですが、CAPD患者さんでのバンコマイシン投与設計はどのように行えば良いのか悩む時が多いです。特に腹膜炎でのCAPD内にバンコマイシンを混注する場合や、敗血症で全身投与する場合もあり状況に応じての投与設計をどうすれば良いか悩んでおります。母集団解析ソフトにはこのような患者は含まれていないと思うのですが、ccr6ml/min前後としてある程度の参考にして考える場合もあります。
何か投与設計するときのコツはありますでしょうか。血液透析患者さんのように決められた一定量を投与する方法等があるのでしょうか。
小生のような未熟者ですが、ご教示いただけますと幸いです。
A.講演で私がご提示した20mg/kg loadingから、毎日7.5-10mg/kg維持で投与計画を行い、そのあとの血中濃度でフォローする方法はあくまでサブラッドのような置換液を20L/日使用した無尿のCHDF患者の場合です。いわゆる日本で行われているCHDF患者さんの典型です。
施設によってCHDFのやり方が異なる場合、例えば20L/日ではなく30L/日の補液を使っていれば、投与量は私の示した典型の1.5倍必要です。また患者さんの尿量があり、患者さん自身のGFRが14mL/minで、置換液使用量が同じ20L/日であればCHDFクリアランスが14mL/minですので、加えるとGFR28mL/minの高度CKD患者の用量と同じになり、この場合の投与量は私の示した典型の2倍必要になりますが、これらは山本武人先生のクリアランス理論と同じ考え方です。一応、抗菌薬TDMガイドライン2022ではeGFR<30mL/min/1.73m2では「バンコマイシンの適応としない」となっていますが、これは投与してはいけないというものではなく、化学療法学会でも腎機能が低下してもバンコマイシンを好んで使う感染症専門医もいらっしゃいます。
CAPD患者さんでMRSA腹膜炎では腹腔内にバンコマイシンを有効濃度に保つには局所投与になるので、15~30mg/kgを5~7日毎で十分だと思いますが、MRSA敗血症や肺炎となると全身投与が必要になります。PBRが34-55%なので腹腔内投与しても半分くらいしか血中に移行しないですし、腹膜への刺激性を考慮すると腹膜炎以外ではあまり抗菌薬の腹腔内投与はしたくありません。血清Cr値が同体型のHD患者さんと同等であれば、ほぼHD患者と同じ用量でよいはずです。血清Cr値が同体型のHD患者さんよりも高く、例えば15mg/dLと高値の男性であれば、そのCAPD患者さん自身の腎機能は低いと思います(いずれHD+CAPD療法が必要になり、やがてHDに完全移行することになるでしょう)。厳密にCAPD患者さんの腎機能を知ろうとすれば、CAPD患者さんの24時間畜尿CCrを測定するとよいでしょうが、ふつうそこまではせず、バンコマイシンのTDMを実施して予測した濃度よりも高ければ腎機能が予想したよりも低い、というように判断して投与設計しなおすのが一般的なやり方だと思います。

