◆連載◆クロストリディオイデス・ディフィシル(CD)腸炎について考える 第9回 前編
1.クロストリディオイデス・ディフィシル(CD)腸炎・偽膜性大腸炎とバンコマイシンのTDM
(1)はじめに
今回は抗菌薬関連下痢症・細菌性腸炎の原因菌として最も重要なクロストリディオイデス・ディフィシル感染症Clostridioides difficile(CD)腸炎について我々の経験した症例について解説したい。これも腸内細菌叢の変化が大きく関わる疾患である。なおCDは2016年まではクロストリジウム・ディフィシルと呼ばれていた有芽胞偏性嫌気性グラム陽性桿菌で下痢、腹痛、発熱を伴うCD腸炎や偽膜性大腸炎、あるいは麻痺性イレウスや巨大結腸症発症、腸管穿孔の主要な原因菌とされ、健康成人でも日本人で10~50%前後の糞便から検出され、もともと弱毒菌で菌量が少なければ健常者には病原性はないが、菌量が増えてトキシンA、トキシンBという外毒素を産生すると、腸炎を引き起こす。傷口から感染しやすい破傷風菌 (C. tetani )、真空パックの食品内部でも増殖して食中毒の原因になるボツリヌス菌 (C. botulinum )、常在菌だが毒素を産生して食中毒の原因になり、ガス壊疽菌を起こすことがあるウェルシュ菌 (C. perfringens )などは今まで通りClostridium属である。
(2)症例1)
68歳、体重56.8kgの男性透析患者で原疾患は糖尿病。肛門周囲膿瘍のため入院し、セフォチアムに次いでクリンダマイシン+セフタジジムが投与された。第23病日に発熱、白血球数29,190/μL、CRPが20mg/dLを超え、大腸ファイバーにて著明な偽膜*(図1左)の形成、CD抗原を認めたため、抗菌薬投与を中止し、バンコマイシン(VCM)散0.5gを1日4回、経口投与された。翌日よりメトロニダゾール250mg、1日2回を経口投与後、8日目にCD抗原は消失し投与10日目には内視鏡にて偽膜形成の減少が観察された(図1中)。しかし下痢症状の改善があまりみられなかったことから、36病日(VCM投与14日)に血漿VCM濃度の測定を依頼すると51.98μg/mLと異常高値であり、便培養でCDが検出されなかったためVCMの投薬を中止して経過を観察した。37病日には58.74μg/mL(経口VCM投与後では当時の世界記録)と非常に高値を示した。 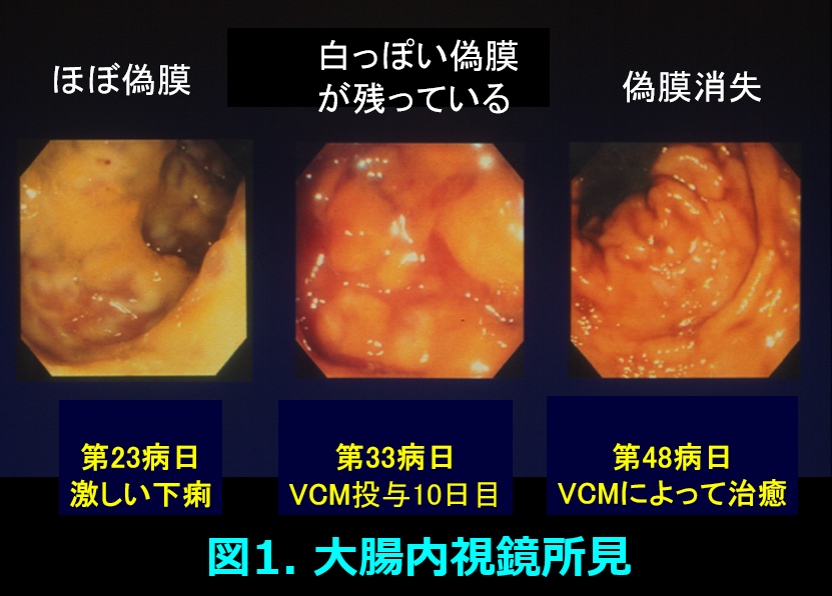 投与中止後6.56μg/mlにまで血漿濃度が低下するのに27日間を要し、この間のVCMの消失半減期は158時間であり、Vdを0.956L/kgとしてクリアランスを算出するとClearance =(ln2×Vd)/t1/2 =(0.693×0.956×56.8×1000)/158×60=3.97mL/minと透析患者のVCMクリアランスが非常に低いことも解明された。さらに158時間という半減期から58.7μg/mLという濃度は完全に定常状態に達しているわけではないが、バイオアベイラビリティ(この場合、吸収率)=Clearance×steady state serum VCM level/ VCM dose= (3.97×58.7)/{2.0×1,000,000/(24×60)}=0.1678となり、吸収されるはずのないVCMが偽膜という腸管炎症所見が強い場合、少なくとも16.78%が吸収されたと考えられた。これはCDトキシンが腸管上皮の緻密結合tight junctionを傷害してバリア機能が破綻したために、吸収されるはずのないVCMが吸収されたものと考えた。VCMの中毒反応は腎障害や聴覚障害が知られているが、腎機能の廃絶したこの症例には有害反応は見られなかった。48病日には偽膜は完全に消失した(図1右)。
投与中止後6.56μg/mlにまで血漿濃度が低下するのに27日間を要し、この間のVCMの消失半減期は158時間であり、Vdを0.956L/kgとしてクリアランスを算出するとClearance =(ln2×Vd)/t1/2 =(0.693×0.956×56.8×1000)/158×60=3.97mL/minと透析患者のVCMクリアランスが非常に低いことも解明された。さらに158時間という半減期から58.7μg/mLという濃度は完全に定常状態に達しているわけではないが、バイオアベイラビリティ(この場合、吸収率)=Clearance×steady state serum VCM level/ VCM dose= (3.97×58.7)/{2.0×1,000,000/(24×60)}=0.1678となり、吸収されるはずのないVCMが偽膜という腸管炎症所見が強い場合、少なくとも16.78%が吸収されたと考えられた。これはCDトキシンが腸管上皮の緻密結合tight junctionを傷害してバリア機能が破綻したために、吸収されるはずのないVCMが吸収されたものと考えた。VCMの中毒反応は腎障害や聴覚障害が知られているが、腎機能の廃絶したこの症例には有害反応は見られなかった。48病日には偽膜は完全に消失した(図1右)。
下痢症状は改善したが、57病日(VCM投与中止24日目)に気管支炎を発症したため、レボフロキサシン投与を行ったところ、下痢・発熱の再発がみられ、再びCD抗原が認められた(図2)。VCM再投与に至ったが、VCMの血漿濃度は一貫してCDのMICである0.78μg/mlを大きく上回っていたにもかかわらず、腸炎が再発したため、血中から腸管内へのVCMの移行は不良な可能性が示唆された。以上のことから、血液透析患者にVCM散を長期投与する際には血中漿濃度モニタリングを行う必要性があると思われた。 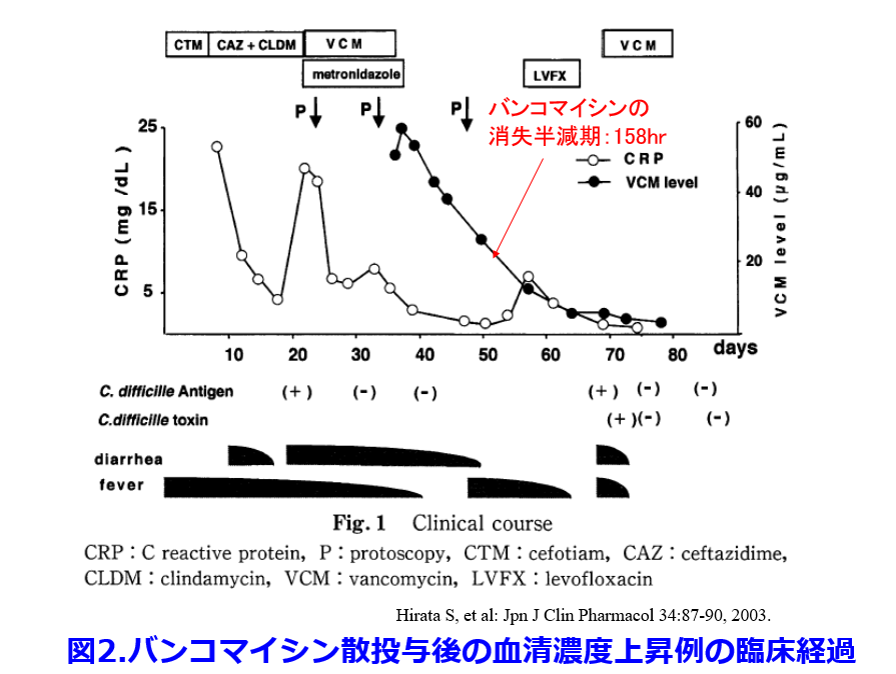 偽膜:大腸粘膜膜表面に血漿内のフィブリンや好中球、粘液などの炎症性物質が浸みだして凝固壊死して作られる膜のようなもの、わかりやすく言うとかさぶたのようなもの。CDだけでなく赤痢菌やカンジダなどによっても形成される。正常な大腸はオレンジ色に見えるが、偽膜は黄白色の扁平あるいは半球状の低い隆起をなす。
偽膜:大腸粘膜膜表面に血漿内のフィブリンや好中球、粘液などの炎症性物質が浸みだして凝固壊死して作られる膜のようなもの、わかりやすく言うとかさぶたのようなもの。CDだけでなく赤痢菌やカンジダなどによっても形成される。正常な大腸はオレンジ色に見えるが、偽膜は黄白色の扁平あるいは半球状の低い隆起をなす。
(3)その後の院内アウトブレイク
この症例が治癒後、院内感染によってCD腸炎患者は同じ病棟内で合計16名となったが、全員が発症前に抗菌薬を投与されており、抗菌薬の併用はCD感染症の治癒率を低下させることが明らかになっている2)。H2ブロッカーのファモチジン、ラニチジン、プロトンポンプ・インヒビター(PPI)のランゾプラゾールといった胃酸分泌抑制薬9名および制酸薬服用者3名で16名中12名(75%)で、同施設内の全透析患者における38.3%に比べ高かかったことから、胃酸抑制が腸炎の発症に関与している可能性が考えられた。さらにある大学に依頼したCDの遺伝子検査結果によると全員が初発の偽膜性腸炎患者と同じCDであり、16名全員が院内感染であることが判明した。
経口VCMの推奨量は0.5-1g/日の7-10日投与(添付文書用量は1回0.125~0.5gを1日4回)で、Keighleyら3)は0.125gの4回/日投与で十分な便中濃度を保ったとしている。本症例は重篤であったため、1日2.0gの投与に踏み切ったが、CD感染に対してVCMの大量投与は腸内細菌叢を崩壊する可能性があるため、少量の方がよかったかもしれない。
(4)クロストリディオイデス・ディフィシル(CD)腸炎とは
抗菌薬投与によってCDが異常増殖し、免疫能の低下した高齢者・手術侵襲・TPNによる粘膜退行・腸虚血・血圧低下などの要因が加わると激しい腸炎を発症することがある。ただし通常の状態では他の常在菌の存在がCDの増殖を抑制しているため、CDの菌数は糞便中102/g以下と少なく、毒素を産生して病原性を発揮することはない。抗菌薬の投与による菌交替現象から腸内細菌叢microbiotaが撹乱され、CDの異常増殖が起こり105/g以上になると大量の毒素を産生してCD腸炎が起こる。偽膜性大腸炎はCD腸炎の重症型であり、トキシンによる大腸の炎症粘膜に壊死白血球が集まって偽膜を形成する。CDは芽胞*(図3)を形成するためエタノール消毒でも死なないし、胃酸によっても芽胞を形成している場合は死滅せず、小腸に移行して嫌気性下になると発芽する。免疫能の低い透析患者や超高齢者の病棟では接触感染によって院内感染が起こるとCDトキシンによる腸炎によって重篤な下痢を起る患者が増える始末が悪い菌になる。 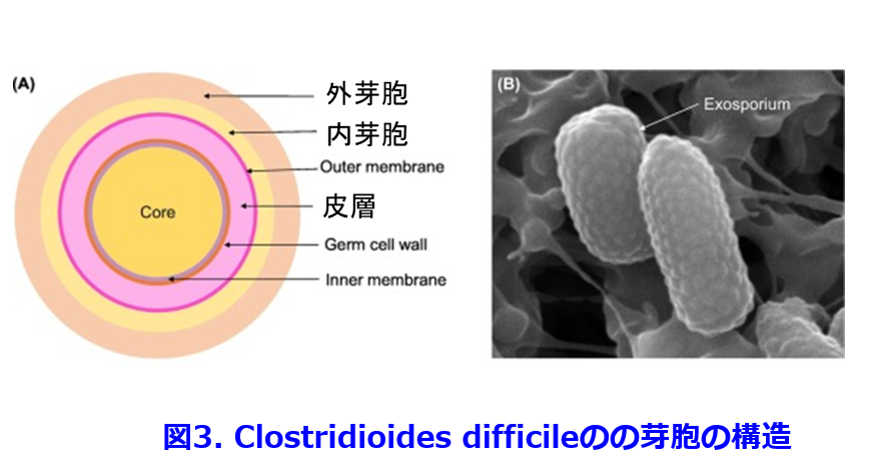 芽胞:ある種の細菌は乾燥や高温、酸や化学物質、紫外線などで環境条件が悪くなると芽胞とよばれる耐久器官を作って生きのびる。この芽胞を形成する菌で好気性の細菌をBacillus属,嫌気性の細菌をClostridium属と呼ぶ。芽胞形成菌であっても周りの環境が生存に適するようになると栄養型になって発芽し分裂増殖を始める。芽胞は代謝が行われていない仮死状態で生物活性がほとんど見られなくなる。
芽胞:ある種の細菌は乾燥や高温、酸や化学物質、紫外線などで環境条件が悪くなると芽胞とよばれる耐久器官を作って生きのびる。この芽胞を形成する菌で好気性の細菌をBacillus属,嫌気性の細菌をClostridium属と呼ぶ。芽胞形成菌であっても周りの環境が生存に適するようになると栄養型になって発芽し分裂増殖を始める。芽胞は代謝が行われていない仮死状態で生物活性がほとんど見られなくなる。
引用文献
1) Hirata S, et al: Jpn J Clin Pharmacol 34:87-90, 2003.
2) Mullane KM et al : Clin Infect Dis Sep 1; 53:440, 2011
3) Keighley MR, et al: Brit Med J 2: 1667-1669, 1978

